실험 - 액체 증기평형
 등록일 / 수정일
등록일 / 수정일 페이지 / 형식
페이지 / 형식 자료평가
자료평가 구매가격
구매가격
- 2009.11.05 / 2019.12.24
- 10페이지 /
 hwp (아래아한글2002)
hwp (아래아한글2002) - 평가한 분이 없습니다. (구매금액의 3%지급)
- 2,000원
최대 20페이지까지 미리보기 서비스를 제공합니다.
자료평가하면 구매금액의 3%지급!
 1
1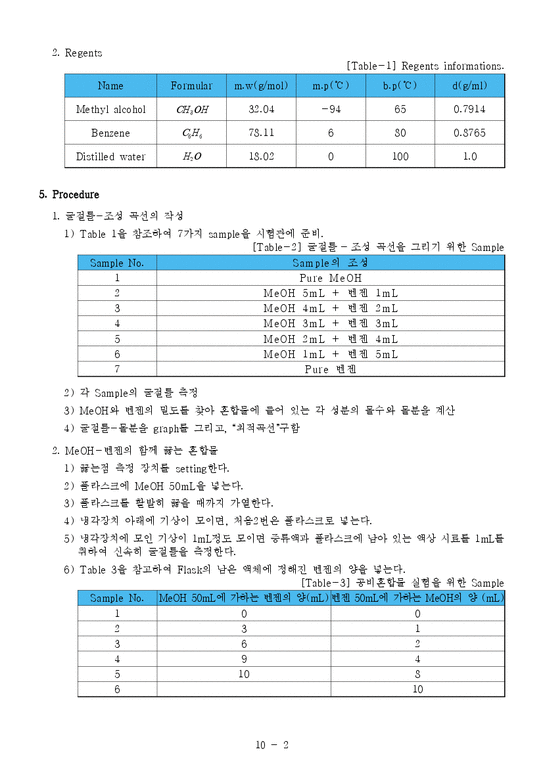 2
2 3
3 4
4 5
5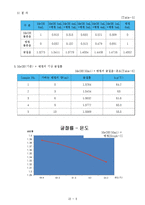 6
6 7
7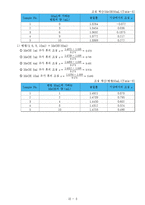 8
8 9
9 10
10
추천 연관자료
- 목차
-
1. Title
2. Purpose
3. Principle
4. Apparatus & Regents
5. Procedure
6. Description
7. Result
8. Error & Cause
9. Discussion
10. Reference
11. Cowoker
- 본문내용
-
1. Title
액체 - 증기 평형(Vapor - Liquid Equilibrium)
2. Purpose
함께 끓는 혼합물의 온도 - 조성 기액평형도를 결정하는데 있다.
3. Principle
이상적인 이성분 혼합물은 전 조성 범위에서 Raoult's 법칙을 만족한다.
Raoult's 법칙
기상에서 성분의 부분압(증기압)은 액상에 있는 성분의 몰분율과 순수한 성분의 포화 증기압의 곱과 같다.
Dalton’s 법칙
는 기상에서의 성분의 몰분율과 전압의 곱과 같다. 그러나 비이상계에서는 Raoult's 법칙에
대해서 양(+) 혹은 음(-)의 편기를 나타낸다. 이성분 혼합물의 성분에 대한 증기압 곡선을 보면 (+)편기는 , 간의 분자 간 상호작용이 분자간 상호작용보다 강할 때 나타난다. (-)편기는 일 때 나타난다. 이러한 편기가 충분히 클 때 전압곡선에서 최대점이나 최소점이 생기게 된다.
액상과 기상의 평형에서의 압력 - 조성의 기액평형도는 다음과 같다.
여기서 는 Raoult's 법칙으로 구할 수 있으나 실제로는 온도 - 조성의 기액평형도를 많이 이용한다. 압력 - 조성의 기액평형도를 뒤집으면 온도 - 조성의 기액평형도가 된다.
끓는점에서의 액상과 기상의 굴절률을 측정하고 표 1의 굴절률을 측정하여 굴절률대 몰분율의 검양곡선을 그리고 검양곡선에서 굴절률(액상, 기상 모두)에 대한 몰분율을 찾는다
4. Apparatus & Regents
1. Apparatus
1) Cottrell melting point measurement equipment
2) Thermometer
3) Stand
4) Clamp
5) Heater
6) Rubber stopper
7) Pipette
8) Boiling chips
9) Refractometer
2. Regents
[Table-1] Regents informations.
Name
Formular
m.w(g/mol)
m.p(℃)
b.p(℃)
d(g/ml)
Methyl alcohol
32.04
-94
65
0.7914
Benzene
78.11
6
80
0.8765
Distilled water
18.02
0
100
1.0
5. Procedure
1. 굴절률-조성 곡선의 작성
1) Table 1을 참조하여 7가지 sample을 시험관에 준비.
[Table-2] 굴절률-조성 곡선을 그리기 위한 Sample
Sample No.
Sample의 조성
1
Pure MeOH
2
MeOH 5mL + 벤젠 1mL
3
MeOH 4mL + 벤젠 2mL
4
MeOH 3mL + 벤젠 3mL
5
MeOH 2mL + 벤젠 4mL
6
MeOH 1mL + 벤젠 5mL
7
Pure 벤젠
2) 각 Sample의 굴절률 측정
3) MeOH와 벤젠의 밀도를 찾아 혼합물에 들어 있는 각 성분의 몰수와 몰분율 계산
4) 굴절률-몰분율 graph를 그리고, “최적곡선”구함
2. MeOH-벤젠의 함께 끓는 혼합물
1) 끓는점 측정 장치를 setting한다.
2) 플라스크에 MeOH 50mL을 넣는다.
3) 플라스크를 활발히 끓을 때까지 가열한다.
4) 냉각장치 아래에 기상이 모이면, 처음2번은 플라스크로 넣는다.
5) 냉각장치에 모인 기상이 1mL정도 모이면 증류액과 플라스크에 남아 있는 액상 시료를 1mL를 취하여 신속히 굴절률을 측정한다.
- 참고문헌
-
1. 위키 백과사전
2. 네이버 백과사전
자료평가
-
아직 평가한 내용이 없습니다.










