레포트 (17,011)

![]() [화학공학] 혼합조 - 유입속도, 탱크용량, 초기농도에 따른 응답특성의 변화를 측정
[화학공학] 혼합조 - 유입속도, 탱크용량, 초기농도에 따른 응답특성의 변화를 측정
반응기의 초기농도와 부피, 유입속도에 영향을 받는데 반응기의 초기농도가 작고 부피가 작을수록, 유입속도가 클수록 변화량이 커진다6.참고문헌․ 화공실험1 매뉴얼․ 강성주, 선우창신, 유의연, 유민수 공역 “화학공정제어”․ 네이버 지식검색 “혼합조 실험”,“전도도”, “농도와 전도도”
8페이지 | 1,500원 | 2013.12.23

화학반응열의 측정과 Hess의 법칙1. Abstract (요약)대부분의 화학반응이 진행되는 동안에는 열의 흡수 또는 방출이 수반된다. 화학 반응시에 방출되는 열량을 각 물질의 엔탈피를 계산하여 예측할 수 있다. 그러나 흑연을 태워서 일산화탄소를 얻는 반응과 같이 엔탈피를 실험적으로 구하기 어려운 경우
7페이지 | 1,500원 | 2013.12.23
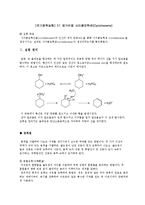
![]() [유기화학실험] E1 제거반응 사이클로헥센(Cyclohexene)
[유기화학실험] E1 제거반응 사이클로헥센(Cyclohexene)
유기화학실험 E1 제거반응 사이클로헥센(Cyclohexene) 실험 목표사이클로헥산올(cyclohexanol)과 인산의 제거 반응(E1)을 통해 사이클로헥센 (cyclohexene)을 생성시키고, 실제로 사이클로헥센(cyclohexene)이 생성되었는지를 확인해본다.Ⅰ. 실험 원리알켄, 즉 올레핀을 합성하는 데 가장 일반적이고 유용한 방
13페이지 | 2,000원 | 2013.12.23

![]() [화학실험보고서] 수소이야기 - 수소가 어떻게 발견되었는지 재현해 보고, 수소의 반응성, 선스펙트럼 등
[화학실험보고서] 수소이야기 - 수소가 어떻게 발견되었는지 재현해 보고, 수소의 반응성, 선스펙트럼 등
속도)로 나타낼 수 있다. 빛의 속도는 일정하므로 파장이 짧은 보라색 빛은 큰 진동수를 가진다. 식 (5)에서 큰 진동수의 빛이 방출되기 위해서는 떨어지는 에너지 준위 차가 커야한다. 가시광선 영역에서 전자가 떨어지는 지점은 n=2인 지점으로 일정하다. 이는 에너지 준위 차가 크기 위해서는 전자가
7페이지 | 1,500원 | 2013.12.23

![]() [일반화학실험] 반응 메카니즘 - 할로겐화알킬의 가수분해
[일반화학실험] 반응 메카니즘 - 할로겐화알킬의 가수분해
일반화학실험 반응 메카니즘 - 할로겐화알킬의 가수분해1. INTRODUCTION이번 실험에서 우리가 알고자 하는 것은 바로 반응 메카니즘이다. 그렇다면 반응 메카니즘이란 무엇인가. 우선 원리와 실험에 들어가기에 앞서서 우린 그것을 알아야 할 것이다. 반응 메카니즘은 전체 반응의 속도법칙을 설명하기
4페이지 | 1,200원 | 2013.12.23

일반생물학실험기질농도에 따른 효소의 반응속도Ⅰ. 서론어떤 물질들이 생명체내에서 동화와 이화작용을 통하여 분해하거나 분해된 물질로부터 새로운 물질을 만들어내는 화학반응을 일으키는 과정을 물질대사라 한다. 이 물질대사가 원활하게 생체내에서 움직일 수 있도록 도와주는 촉매와 같
6페이지 | 1,500원 | 2013.12.23

거치지 못했음에도 오차가 크지 않았던 이유는 젖은 거름 종이를 이용하여 오차를 보정해주었기 때문이다.8.참고 문헌http://kowon.dongseo.ac.kr/%7Eccpark/root/organ/orex08ob.htmEXPERIMENTAL ORGANIC CHEMISTRY - A Small-Scale Approach 유기화학실험유기화학 - 이창규, 한인숙 공역유기화학 실험- 허태성외 편저 녹문당
5페이지 | 1,500원 | 2013.12.23

![]() 유기화학실험 - E2반응으로 cyclohexene을 합성
유기화학실험 - E2반응으로 cyclohexene을 합성
끓는 cyclohexene이 증기가 되어 나오려 할 때 그에 비해 낮은 온도의 공기에 의해 다시 응축되어 밑으로 떨어진다는 것이다. 8. REFERENCE․ 유기화학실험, 양정봉 외 4명․ 다시 쓴 유기화학실험, 김홍범, 자유아카데미, 2004․ Organic chemistry, John McMurry, BROOKS/COLE, sixth edition․ NAVER 백과사전․ 수업 中 필기
7페이지 | 1,500원 | 2013.12.23

반응에서 입체화학을 보면 친핵체가 이탈하는 할로젠화물의 경로를 방해하지 않도록 배후에서 공격한다. 만약 할로젠화 알킬이 광학적으로 활성이면 Sn2 반응시 광학활성도를 그대로 보존하지만 배열이 반전된다. Sn2의 반응속도는 두반응물이 관여한 1단계과정이므로 할로젠화알킬과 친핵체의 두 농
4페이지 | 1,200원 | 2013.12.23

반응은 속도가 느리기 때문에 충분히 오랫동안 저어주면서 가열해야 한다. 2) 젓기는 반응물들이 잘 섞이도록 해주며, 반응속도를 증가시킬 뿐 아니라, 과열이나 갑작스런 끓어 오름(bumping) 을 방지한다 3) 가열하는 동안 거품이 일면 혼합물이 과열된 경우이므로 혼합물이 갑자기 끓지 않도록 주의한
9페이지 | 1,800원 | 2013.12.23





 영역
영역 







