레포트 (450)

화학 실험 보고서1. Abstract이번 실험은 고체 수산화 나트륨과 염산의 중화 반응을 한 단계 및 두 단계로 진행시켜 각 단계의 반응열을 측정하고 이를 통해 헤스의 법칙을 확인하는 실험이다. 헤스의 법칙이란 “엔탈피는 상수 함수이기 때문에 초기에서 최종 상태로 갈 때의 엔탈피 변화는 경로에 무관
4페이지 | 700원 | 2007.10.27

![]() [열역학] Calculation of Joule-Thomson inversion curves for two-phase mixtures
[열역학] Calculation of Joule-Thomson inversion curves for two-phase mixtures
엔탈피적으로 팽창되면서 압력 강하와 함께 온도 변화가 일어나는 현상Theory목 차이 론본 론예 시목 표Thermodynamics반전 온도란?실제 기체의 Joule Thomson 효과는 각 기체에 특유한 어느 온도 이하에서는 냉각, 그 온도 이상에서는 발열을 나타낸다. 이 온도를 반전 온도 혹은 반전 온도라 한다. 목
16페이지 | 1,300원 | 2015.06.01

![]() [화학실험] [물리화학실험] 열량계법을 이용한 용해열 측정
[화학실험] [물리화학실험] 열량계법을 이용한 용해열 측정
1. 실 험 제 목 열량계법을 이용한 용해열 측정2. 실 험 일 시2005년 4월 21일 목요일3. 실 험 목 적 간단하게 만든 열량계로 여러 가지 염들의 용해열을 측정한다. 4. 이 론 적 배 경어떤 물질은 녹을 때 열을 방출하며, 또 어떤 물질은 녹을때 열을 흡수한다. 용해과정에서의 엔탈피의 변화를 용해열(Heat
9페이지 | 1,500원 | 2007.06.01
![]() [열동력실험] 히트 펌프를 이용한 냉난방 사이클 성능 실험
[열동력실험] 히트 펌프를 이용한 냉난방 사이클 성능 실험
엔탈피(h)값 구하기먼저 압력게이지에 측정된 값은 gage압력이므로 대기압인 0.10MPa를 더해준다. 그리고 각각의 엔탈피 값은 R22의 p-h선도를 참고하여 그래프상의 해당 지점을 찾는 방법으로 구했다. 이 방법은 눈으로 측정하기 때문에 정확한 값을 알 수 없었다. 그래서 보완책으로 인터넷의 propath프로그
13페이지 | 1,400원 | 2010.08.14
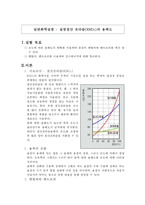
일반화학실험 - 실험질산 포타슘(KNO3)의 용해도Ⅰ.실험 목표1) 온도에 따른 용해도의 변화를 이용하여 물질의 엔탈피와 엔트로피를 계산 할 수 있다.2) 엔탈피, 엔트로피를 이용하여 깁스에너지에 대해 알아본다.Ⅱ.이론1. 시료조사 - 질산포타슘(KNO3)KNO3의 화학식을 가지며 무색의 기둥모양 결정 또
6페이지 | 1,500원 | 2017.03.17

년 화공열역학 2012 1. 실제 기체의 압력이 에 접근할 때 잔류 특성 0잔류 엔탈피와 잔류 엔트로피 모두 에 접근한다 0 .평형의 의미 2.미시적인 척도에서는 변화가 있지만 거시적인 척도에서는 변화가 없는 상태열역학 모델을 이용하여 상평형 계산을 수행하려고 할 때 3.응용 계와 모델의 조합물
18페이지 | 5,500원 | 2024.02.21

- 질산포타슘의 용해도실험목적 → 질산포타슘의 온도에 따른 용해도의 변화를 측정하여 용해열을 구하고, 엔탈피와 엔트로피를 이해한다.실험원리→ 용해도, 화학평형, 깁스에너지, 엔탈피, 엔트로피실험기구 및 시약→ 질산포타슘(혹은 질산칼륨), 메스실린더, 가열기, 온도계, 스탠드, 클램프
10페이지 | 1,500원 | 2013.12.23

![]() 연세대 고려대 성균관대 한양대 기계공학 대학원 구술면접자료 및 공부
연세대 고려대 성균관대 한양대 기계공학 대학원 구술면접자료 및 공부
엔탈피가뭐예요?A : 주로 개방계해석을 할때 출입하는 유체의 내부에너지와 유동일이라고 하는 pv항을 더한형태의 에너지입니다.Q : 그럼 비압축성유동에서 엔탈피는 뭐의함수예요?A : 비압축성유동에선 압력의 영향이 적지만, 실제로는 압력과 온도의 함수입니다.Q : 카르노사이클은 뭔가요?A : 두개
100페이지 | 5,000원 | 2023.11.12

엔탈피-R134a의 엔탈피는 열역학 상태량 표와 PH선도를 이용하여 구한다. (응축기의 입․출구와 증발기의 입․출구 온도 기준)-34 과정은 등엔탈피 과정이므로 같은 엔탈피 값을 갖는다.엔 탈 피kJ/kg1st2nd3rd404.48404.57404.23452.64454.67455.51260263267260263267b. 응축기- 냉각수는 응축기 내에서 온도
24페이지 | 1,800원 | 2006.07.20

엔탈피는 일정한 압력 하에서의 반응열과 같으므로 다음과 같이 쓸 수 있다.△H=q△H는 J/mol 이므로 △H = Q/mol 으로 계산할 수 있다. 따라서 위의 자료들을 이용하여 발생한 열을 구하고, 그것을 NaOH의 몰수로 나누어 엔탈피를 구할 수 있다. 이 때 물의 질량은 최종 비커 질량에서 처음 비커 질량,
3페이지 | 800원 | 2007.10.08





 영역
영역 







