레포트 (450)

엔탈피-R134a의 엔탈피는 열역학 상태량 표와 PH선도를 이용하여 구한다. (응축기의 입․출구와 증발기의 입․출구 온도 기준)-34 과정은 등엔탈피 과정이므로 같은 엔탈피 값을 갖는다.엔 탈 피kJ/kg1st2nd3rd404.48404.57404.23452.64454.67455.51260263267260263267b. 응축기- 냉각수는 응축기 내에서 온도
24페이지 | 1,400원 | 2006.03.24

엔탈피가 중요한 양이다. 엔탈피는 물질의 열 함량을 나타내는 것으로 대개 열적 증감의 변화를 나타내는데 사용한다. 엔탈피는 상태함수이기 때문에 반응물과 생성물의 엔탈피를 알면 어느 화학 변화에 대한 엔탈피 변화를 계산할 수 있게 되며, 출발 물질과 최종 물질이 같은 경우에는 어떤 경로를
5페이지 | 1,200원 | 2014.06.16

엔탈피(h)를 구한다. ☞ 엔탈피를 구하기 위해서는 수증기표를 참고해야 한다. 여기서 중요한 것은 출구온도와 입구온도는 액체상태의 온도이다. 따라서 수증기표에서는 액체상태에서 엔탈피를 찾아야 하는데, 액체상태에는 수증기표에서 세밀하게 나와있지가 않다. 그러므로 엔탈피 차이가 거의 없
13페이지 | 1,400원 | 2010.07.13

엔탈피의 그래프의 기울기를 나타낸다.위의 그래프에서 위쪽의 커브는 물의 포화 엔탈피를 나타내고 아래에 있는 커브는 공기의 엔탈피를 나타낸다. 엔탈피 사이의 간격으로 만들어지는 두 곡선 사이의 면적이 바로 냉각탑의 특성치를 나타내는 것이다.이에 공기의 엔탈피는 냉각탑 단 내에서 물과
38페이지 | 3,500원 | 2006.09.16
![]() [공학실험] Heat Pump(냉동) 사이클의 특성 및 종류 몰리에르선도
[공학실험] Heat Pump(냉동) 사이클의 특성 및 종류 몰리에르선도
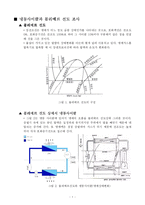
엔탈피는 증가해 간다. 또 냉매액은 점점 증발하여 가스가 되기 때문에 건조도는 높게 되어 차차 포화증기선으로 접근해 간다.그림 . 몰리에르선도와 냉동사이클(냉매상태변화)• 압축기는 증발기에서 포화증기가 된 냉매가스를 흡입하지만, 이것에 압축열이 가해지기 때문에 압력도 엔탈피도 증가
16페이지 | 1,500원 | 2007.01.04

엔탈피(Enthalpy)가 무척 중요하다.(엔탈피는 그리스어 enthalpein(=열)에서 유래되었다.)엔탈피는 미국의 물리화학자인 J Willard Gibbs에 의해 제시되었다. 엔탈피는 상태함수로 다음과 같이 정의된다. H = U + PV (U : 계의 내부에너지)(엔탈피에 관한 자세한 개념은 뒤의 Discussion에서 다루기로 하자.)엔탈피는 열
4페이지 | 1,200원 | 2014.01.14

![]() [액체 및 고체연로의 발열랑 측정] 액체 및 고체연로의 발열랑 측정
[액체 및 고체연로의 발열랑 측정] 액체 및 고체연로의 발열랑 측정
엔탈피와 반응물의 엔탈피 차이로써 표시된다. 즉,한 개 이상의 반응물이 연소되어 한 개 이상의 생성물로 되었을 때, hRP를 연료의 mole당 연 소 엔탈피라 하면, bar hRP = hp -hR = SUM from P nebar hf DEG +DELTAbar he -SUM fromRne bar hf DEG + DELTAbar hi 식(6. 1)로 표시된다. 여기서 P와 R는 생성물과 반응
6페이지 | 800원 | 2007.04.08

![]() [화학공학 프로그램] GTL 기술을 사용하여 가스화 방식별 개념 설계
[화학공학 프로그램] GTL 기술을 사용하여 가스화 방식별 개념 설계
엔탈피 DELTA barH ` H 2 O ``=` DELTA barH ` (l) `+ DELTA barH ` vap,H 2 O `+ DELTA barH ` (g) ``=`5.6550`+`40.656`+`26.5166=72.8276(kJ/mol)○ 메탄의 엔탈피 DELTA H vap,C`H 4 =43.572(kJ/mol)○ Vapor의 총 엔탈피 DELTA barH ` vap `=` DELTA barH ` (l) `+ DELTA barH ` vap,H 2 O `+ DELTA barH ` (g) ``+ DELTA barH ` C`H 4 `
31페이지 | 2,500원 | 2013.03.20

1. 요약1. 실험의 목적: 수산화나트륨과 염산의 반응을 통해 헤스의 법칙이 상태 함수임을 확인한다.2. 실험 방법ㄱ. 첫 번째 엔탈피의 측정a. 250ml 비커를 씻어서 말린 후에 무게를 측정하고 스티로폼 컵에 담아서 단열의 상 태를 만든다. b. 12M 염산용액을 실험 조건에 맞는 0.25M 의 염산용액으로 묽힌
4페이지 | 1,200원 | 2013.12.23

Ⅰ.실험목적헤스의 법칙을 이용하여 반응열을 측정한다.Ⅱ.실험 이론엔탈피(Enthalpy)-화학 반응에서 각 물질들이 가지고 있는 고유한 에너지-H로 나타낸다.△H=생성 물질의 엔탈피 총합 – 반응 물질의 엔탈피 총합△H를 이용해서 반응의 종류를 알 수 있다.화학 반응에서 에너지 변화-계(system):
5페이지 | 1,200원 | 2013.12.23





 영역
영역 







