[식품학] 단백질식품의 조리
 등록일 / 수정일
등록일 / 수정일 페이지 / 형식
페이지 / 형식 자료평가
자료평가 구매가격
구매가격
- 2012.07.25 / 2019.12.24
- 11페이지 /
 hwp (아래아한글2002)
hwp (아래아한글2002) - 평가한 분이 없습니다. (구매금액의 3%지급)
- 1,700원
최대 20페이지까지 미리보기 서비스를 제공합니다.
자료평가하면 구매금액의 3%지급!
 1
1 2
2 3
3 4
4 5
5 6
6 7
7 8
8 9
9 10
10 11
11
추천 연관자료
- 목차
-
단백질식품의 조리
1. 단백질의 특징
2. 단백질의 구조
3. 단백질의 변성
<달걀조리>
<두부조리>
<어패류조리>
<육류의조리>
- 본문내용
-
단백질식품의 조리
1. 단백질의 특징
단백질은 동식물 원형질의 주성분이며 직접 생명현상을 담당하는 중요한 물질이다. EH한 영양적으로 없어서는 안 될 중요한 요소이며 수천에서 수만의 분자량을 가지는 고부자로 독특한 전기적 성질과 가열에 의해 쉽게 변성하는 성질을 가지고 있다. 따라서 단백질을 많이 함유하는 식품은 같은 원료를 사용해도 상당히 다른 음식물을 조리할 수 있다.
2. 단백질의 구조
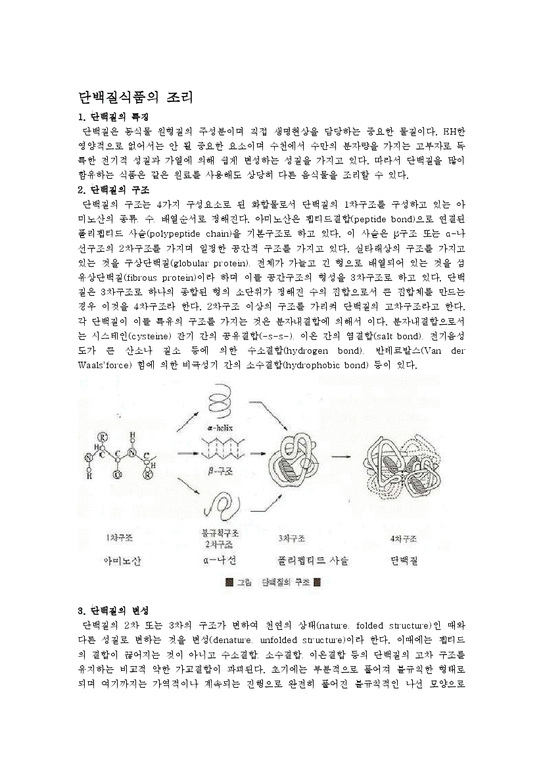
단백질의 구조는 4가지 구성요소로 된 화합물로서 단백질의 1차구조를 구성하고 있는 아미노산의 종류, 수, 배열순서로 정해진다. 아미노산은 펩티드결합(peptide bond)으로 연결된 폴리펩티드 사슬(polypeptide chain)을 기본구조로 하고 있다. 이 사슬은 β구조 또는 α-나선구조의 2차구조를 가지며 일정한 공간적 구조를 가지고 있다. 실타래상의 구조를 가지고 있는 것을 구상단백질(globular protein), 전체가 가늘고 긴 형으로 배열되어 있는 것을 섬유상단백질(fibrous protein)이라 하며 이들 공간구조의 형성을 3차구조로 하고 있다. 단백질은 3차구조로 하나의 종합된 형의 소단위가 정해진 수의 집합으로서 큰 집합체를 만드는 경우 이것을 4차구조라 한다. 2차구조 이상의 구조를 가리켜 단백질의 고차구조라고 한다. 각 단백질이 이들 특유의 구조를 가지는 것은 분자내결합에 의해서 이다. 분자내결합으로서는 시스테인(cysteine) 잔기 간의 공유결합(-s-s-), 이온 간의 염결합(salt bond), 전기음성도가 큰 산소나 질소 등에 의한 수소결합(hydrogen bond), 반데르발스(Van der Waals'force) 힘에 의한 비극성기 간의 소수결합(hydrophobic bond) 등이 있다.
자료평가
-
아직 평가한 내용이 없습니다.










