[열역학] VLE실험 Data로부터 Hexane과 TAME 이성분계의 열역학적인 물성을 분석
 등록일 / 수정일
등록일 / 수정일 페이지 / 형식
페이지 / 형식 자료평가
자료평가 구매가격
구매가격
- 2008.08.22 / 2019.12.24
- 23페이지 /
 hwp (아래아한글2002)
hwp (아래아한글2002) - 평가한 분이 없습니다. (구매금액의 3%지급)
- 2,400원
최대 20페이지까지 미리보기 서비스를 제공합니다.
자료평가하면 구매금액의 3%지급!
 1
1 2
2 3
3 4
4 5
5 6
6 7
7 8
8 9
9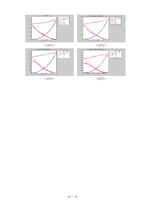 10
10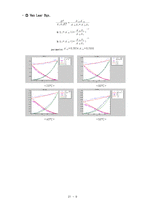 11
11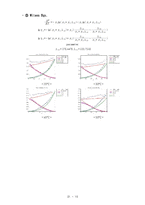 12
12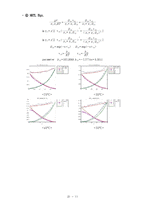 13
13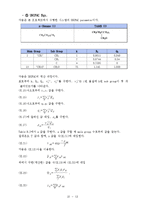 14
14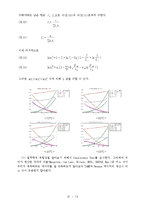 15
15 16
16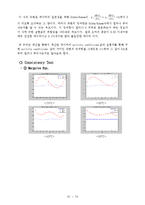 17
17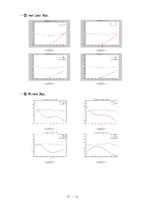 18
18 19
19 20
20
추천 연관자료
- 목차
-
❏ Introduction
❍ 개 요
❍ 목 적(Hexane/TAME계를 선정하게 된 이유)
❍ 방 법
❏ Theory
❍ 활동도 계수와 과잉 Gibbs 에너지에
대한 일반적 고찰
❍ 국부조성 모델 Wilson eqn.
& NRTL eqn.에 대한 고찰
❍ UNIFAC method에 대한 고찰
❏ Procedure / Result / Discussion
❍ VLE DATA Analysis
∙ , , vs 의 그래프
❍ 열역학적 부합성(일관성, Consistency)에
대한 설명
❍ Consistency Test
∙ P-x1-y1 선도
❍ Excess Property (GE, HE, TSE) Plot
❏ Conclusion
❏ Reference
- 본문내용
-
❍ 개 요
VLE실험 Data로부터 Hexane과 TAME 이성분계의 열역학적인 물성을 분석함으로써 알려진 식들의 적합성을 알아보고 P-x1-y1 diagram을 통해 이성분계 분리의 가능성을 예측한다.
❍ 목 적(Hexane과 TAME계를 선정하게 된 이유)
TAME란 함 산소제의 한 종류로 자동차 연료의 개선을 통한 직접적인 공해문제 개선을 위해 만들어졌다. 함 산소연료는 공기연료 혼합기에 산소를 추가한 결과를 가져오기 때문에 완전연소에 보다 가까워 일산화탄소 배출량을 줄여준다.
함 산소제는 알콜과 에테르류로, 현재 가장 많이 사용되고 있는 성분은 MTBE 였으나, 친수성으로 인한 수질오염적인 측면에서 사용이 축소되고 있으며, 최근에는 TAME (tertiary amyl methyl ether)이 사용되고 있다.
에테르류는 isoolefin과 alcohol의 반응에 의해 합성된다. 정확한 에테르의 정제와 oxi-gasolin 의 상변화를 판단하기 위해서는, 혼합물의 열역학적 조성뿐만 아니라 상평형에 대한 지식이 필요하다.
그래서 우리는 TAME (1.1-dimethylpropyl methyl ether) + haxane 을 시스템으로 택하여, VLE실험 data로부터 1.1-dimethylpropyl methyl ether과 haxane 이성분계의 열역학적인 물성을 분석함으로써 알려진 식들의 유용성과 적합성을 알아보고자 한다.
❍ 방 법
어느 상태에서 분리가 잘 일어나는지를 알아보기 위해서 우리는 조성과 상태의 관계를 알아볼 것이다. 이 시스템의 Degree of Freedom은 이다. 즉 이 상태를 규정하기 위해선 2개의 변수에 대한 고려가 있어야 한다. 따라서 우리는 압력, 온도, 조성을 고려할 것이다.
온도와 압력 두 가지를 모두 고려하기는 힘들기 때문에 3가지 경우의 온도(25, 35, 45, 55°C)에서 분리를 한다고 가정하고, 그 온도에서 분리가 가장 잘 일어나는 압력을 찾고자 한다.
압력과 조성의 관계를 밝히려면 의 그래프를 그려야 하는데, 이를 위해서는 Bubble P, Dew P를 찾는 과정을 이용한다. 이를 구하기 위해서 Gamma/Phi Formulation을 이용하는데, 여기에서 TAME에 대한 자료값이 부족하여 Modified Raoult's Law로 그래프를 그렸다.
이 과정에서 activity coefficient 가 필요하다. 이를 구하는 식으로 여러 가지 식들이 제시되는데, 우리는 이번에 Margules, van Laar, Wilson, NRTL 식을 비교할 것이다. 이 식들의 비교를 통해서 식의 유용성에 대해서 알아 볼 수 있을 것이다.
각각의 식 중에서 실험치를 잘 예측할 수 있는 식을 찾고, 그 식을 이용하여 의 그래프를 그릴 것이다. 그리고 과연 분리를 할 수 있는지 그 가능성에 대해서 알아볼 것이다.
- 참고문헌
-
- J. M. Smith, H. C. Van Ness, M. M. Abbott.「Introduction to Chemical Engineering Thermodynamics」 7th ed. , Boston : McGraw-Hill, c2005.
- Robert H. Perry. 「Perry's chemical engineers' handbook」7th ed. , New York : McGraw-Hill, c1997.
- Palm, William J. (William John), 용호택 옮김. 「MATLAB 공학 응용」, 서울 : 아진, 1999
- O'Neil, Maryadele J. 「The Merck index : an encyclopedia of chemicals, drugs, and biologicals」13th ed., Whitehouse Station, NJ : Merck Research Laboratories, c2001.
- 박홍일, 『에탄올 혼합율이 가솔린 엔진의 배기와 성능에 미치는 영향』., 한국해양대 대학원 200402
- Armando del Rio, Baudilio Coto, Concepcion Pando, and Juan A. R. Renuncio,『Vapor-Liquid Equilibria for the Binary System Hexane + 1,1-Dimethylpropyl Methyl Ether at 298.15, 308.15, 318.15, and 328.15 K』, Industrial & engineering chemistry research, 2002, Vol.41 Issue 5, p1364-1369,
- Lohmann, J., Joh, R., Gmehling, J. 『From UNIFAC to Modified UNIFAC (Dortmund) 』, INDUSTRIAL AND ENGINEERING CHEMISTRY RESEARCH
2001, Vol.40 Issue 3, p957-96
자료평가
-
아직 평가한 내용이 없습니다.










