레포트 (471)
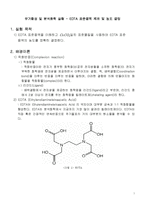
![]() 무기합성 및 분석화학 실험 - EDTA 표준용액 제조 및 농도 결정
무기합성 및 분석화학 실험 - EDTA 표준용액 제조 및 농도 결정
표준용액을 넣으면 EBT에 결합되었던 금속이온이 EDTA와 결합해 EBT 지시약은 떨어져 나간다. 이로 인해 반응종점에서 용액 색깔은 EBT 본래의 색인 푸른색으로 변한다.금속착화물의 안정도 상수가 EDTA 상수의 10분의 1 정도 작아야 적당하기 때문에 일부 금속의 적정에서만 사용할 수 있다. 보통 칼슘과 마
7페이지 | 1,500원 | 2014.06.04

![]() 0.01M EDTA 표준용액 조제․표정 및 물의 경도 측정(전경도,Ca²⁺)
0.01M EDTA 표준용액 조제․표정 및 물의 경도 측정(전경도,Ca²⁺)
용액중에 가하면 킬레이트화를 일으켜, 적색 ~ 적 자색을 띤다.다음에 이 용액 중에 EDTA 표준용액을 적가하면 EDTA가 EBT보다 Ca, Mg의 킬 레이트 화합물을 만들기 쉽기 때문에 Ca, Mg순서로 EDTA와 결합하여 무색의 킬 레이트 화합물이 되고 반응종료와 함께 용액의 색은 유리된 EBT에 의해 청색이 된다.칼슘
10페이지 | 2,000원 | 2015.07.25

I. Introduction• 실험목적정량적 화학반응이 일어나는데 양적 표준이 되는, 농도가 정확한 시약(표준용액)을 만들어본다.II. Procedure• 시약 및 기구1) 시약HCl 염화 수소 수용액. 염화수소산이라고도 하며, 대표적인 강산이다. 때문에 대개 물에희석하여 묽은 염산으로 사용한다. Mw=36.46 g/mol, Bp=110℃, Mp
3페이지 | 800원 | 2014.03.26

![]() [용액][용액의 정의][용액의 중합][표준용액][완충용액][생리적 염류용액]용액의 정의, 용액의 중합, 표준용액, 완충용액, 생리적 염류용액
[용액][용액의 정의][용액의 중합][표준용액][완충용액][생리적 염류용액]용액의 정의, 용액의 중합, 표준용액, 완충용액, 생리적 염류용액
용액의 정의, 용액의 중합, 표준용액, 완충용액, 생리적 염류용액 분석Ⅰ. 용액의 정의Ⅱ. 용액의 중합Ⅲ. 표준용액Ⅳ. 완충용액Ⅴ. 생리적 염류용액참고문헌Ⅰ. 용액의 정의둘 이상의 물질을 함유하고 있는 균일계(기체, 액체, 고체 등 어느 한 가지 상으로 존재하는 계)를 용액(solution)이라고 한다
5페이지 | 5,000원 | 2011.03.24

![]() Preparation and standardization of 0.1N-HCl 0.1 N 염산 표준용액의 조제 및 표준화
Preparation and standardization of 0.1N-HCl 0.1 N 염산 표준용액의 조제 및 표준화
< 실험 보고서 >1. Title : Preparation and standardization of 0.1N-HCl0.1 N 염산 표준용액의 조제 및 표준화2. Date : Name : Co-worker : Weather : Temperature : 19 ℃ Humidity : 37 %3. Object : 이 실험의 목적은 산-염기 중화반응을 이용해서 지시약법, 전위차법, 전기전도도법으로 종말점까지의 적정소비량을 구하여 정량하는 원
15페이지 | 1,500원 | 2011.03.10

표준온도(20°C)의 용적으로 환산한 다음 이 값과 용기의 표기값과의 차를 구한다.원리표준용액(Standard solution)1) 일차 표준용액(primary standard sol)1차 표준물질(표준시약)ⅰ) 순수한 단일 물질로 순도 99.9% 이상ⅱ) 공기 중 수분이나 이산화탄소를 흡수하지 않는 것ⅲ) 산화환원되지 않고 화학조성이
4페이지 | 1,200원 | 2013.12.23

1. SubjectStandard Solution2. object부피법 정량에 의한 물과 폐수의 분석은 정확한 노르말 농도의 (normality) 표준 시약을 사용 함으로서 그 결과를 ㎎/ℓ로 계산하는데 시간을 크게 절약 할 수 있다. 정확한 노르말 농도의 용액을 제조하는 것은 그 논리적 체계를 이용한다면 그리 시간이 걸리는 일이 아니다.
12페이지 | 0원 | 2004.05.19

![]() [화학공학기초실험] 0.1N-H2SO4의 표준용액 제조 및 공업용 가성소다 중의 전체 알칼리 정량
[화학공학기초실험] 0.1N-H2SO4의 표준용액 제조 및 공업용 가성소다 중의 전체 알칼리 정량
실험제목0.1N-H2SO4의 표준용액 제조 및 공업용 가성소다 중의 전체 알칼리 정량실험목적0.1N-H2SO4 표준용액을 제조하여 공업용 가성소다 중의 전체 알칼리를 정량한다초자 및 기구250㎖ mess flask, 비이커, 뷰렛, 세척병, 증류수, 삼각플라스크, 피펫, 저울시약H2SO4-성질순수한 황산은 무색의 점성이 있
6페이지 | 1,500원 | 2013.12.23

![]() [분석화학, 일반 화학] 산, 염기 표준 용액 만들기와 표정
[분석화학, 일반 화학] 산, 염기 표준 용액 만들기와 표정
산, 염기 표준 용액 만들기와 표정1). 실험 목적메스플라스크를 이용하여 산, 염지 적정의 당량점 or 농도를 결정하고 표준 용액을 만들어 본다.지시약의 변화를 관찰하여 산, 염기 적정을 습득 한다. 2).실험 원리* 농도 : 일정량의 용액속에 포함 되어 있는 용질의 양% 농도 = 용질의 질량/ 용액의 질
4페이지 | 500원 | 2009.03.30

![]() 화학기초실험 - M,100 EDTA 표준액을 사용하여 물의 경도(전경도, 칼슘경도)를 측정
화학기초실험 - M,100 EDTA 표준액을 사용하여 물의 경도(전경도, 칼슘경도)를 측정
용액 1~2방울을 넣는다.③ pH10dml 염화암모늄-암모니아 완충용액 1mL를 넣는다.④ EBT지시약을 3~4방울 넣고, 0.01M EDTA 표준용액으로 적정한 후, 소비된 EDTA표준용액의 양을 기록한다.2)칼슘경도① 검수(수돗물) 50mL를 취해 코발트비커에 넣는다.② 검수에 8N-KOH용액 4mL를 넣는다.③ 1N-KCN용액 0.3mL와 10% 염
6페이지 | 1,200원 | 2014.05.20





 영역
영역 







