레포트 (1,236)

부분 중간까지 채우고 액체가 노출된 표면으로부터 증발을 방지하기 위해 뚜껑응 덮고, 항온조 속에 10~15분간 방치하여 온도가 평형에 도달하였을 때 뚜껑을 열고, 마개를 끼운다. 이때 마개 끝으로 유출한 과량의 액체는 거름종이로 조심스럽게 묻혀낸다. 이때 마개 모세관내의 액체가 제거되지 않도
6페이지 | 1,500원 | 2014.06.04

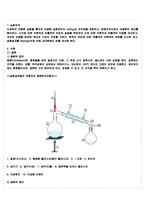
부분이 수직이 되도록 지지대로 항온수조에 고정한다.4) 확산관에 공기나 질소를 흐르게 한다.5) 기체를 흐르게 하여 약 15분 후를 t=0으로 하고 이때의 액체의 위치를 읽어 Z0로 한다. 6) 약 10-15분 간격으로 액체의 위치를 읽는다. 실험은 약 2시간 동안 행한다. 7) 다른 온도에서 위의 실험을 반복한다.5
5페이지 | 1,200원 | 2014.06.04

부분압력의 비와 같다.위에서 말한 것은 일반적인 사항이다. 실제 용액에서 한 성분의 부분압력 P i를 예측하는 방법은 보여 주지 않았다. 1884년에 Raoult은 어떤 용액에 대해서 한 성분의 부분압력은, 순수한 성분의 증기압에 그 성분의 몰분율을 곱한 것과 같다는 것을 알았다.P i `=`x i P i ^AST
13페이지 | 2,000원 | 2014.05.20
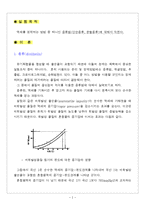
부분압력PA。 : 순수한 A의 증기압NA : A성분의 몰분율NA = nA/(nA + nB + nC + )만약 A 이외의 모든 성분들이 비휘발성 액체라면 혼합물의 전체압력은 비휘발성 화합물의 증기압이 거의 0이기 때문에 성분 A의 부분압력과 동일하다. 따라서 혼합물로부터 증류되어 나온 증류액은 순수한 것이다. 그러나 2
15페이지 | 2,000원 | 2014.05.20

압력을 정확하게 알아내기 위해서는 수증기의 부분압력을 보정해주어야 한다. ② 완전기체 상태방정식- 낮은 압력과 높은 온도에서 기체는 이상기체의 행동을 보인다.PV = nRTR = PV / nT * MPV / wT (n = w/M)( M : 기체 시료의 분자량 w : 기체 시료의 질량 )③ 몰분율과 부분압력1) 몰분율어떤 성분의 몰수(
5페이지 | 1,200원 | 2014.03.26

부분압력을 가지고 기체 혼합물의 성질을 논하였다. 이런 분몰 성질 중에서 가장 쉽게 떠올릴 수 있는 것이 바로 「분몰 부피(Partial Molar Volume)」이다. 왜냐하면 혼합물 시료 중의 한 성분이 전체 부피에 기여하는 부피를 나타내는 것이 바로 「분몰 부피(Partial Molar Volume)」이기 때문이다.ⓑ 몰분율(Mole F
7페이지 | 1,500원 | 2014.03.26

부분에 대한 설명은 Di우리는 직선이라고 가정을 하는데, 모두 곡선이 나3. Procedure/results23(2) Consistency test실제 값과 실험값과의 차이 Gibbs/Duhem 식에 부합하는가를 알아보는 간단한 실험이 consistency test 그림 13: 60℃ Methanol(1) /Water(2) binary
33페이지 | 2,500원 | 2014.01.14

압력에 비례한다는 법칙으로 다음과 같이 표현된다. ◇ C=Hp c = 액체중 기체농도 h = 헨리 상수p = 기체의 분압◇ p=Hx P = 비휘발성 용질의 증기압력,k = 비례상수로 헨리의법칙 상수X = 몰분율적정-일정한 부피의 시료용액 내에 존재하는 알고자 하는 물질의 농도을, 이것과 반응하는 데 필요한 시약
6페이지 | 1,500원 | 2014.01.14

몰분율y : 증기의 몰분율D : 유출되는 액의 몰수dt 시간동안 Total mass balancew 2 -w 1 =dW=-Ddt -D= dW over dt -① Component balanced(Wx) over dt=-DyW BULLET dx over dt +x BULLET dW over dt= -Dy ②①식을 ②식에 대입한다.dW BULLETy=W BULLETdx +x BULLETdW (y-x) BUL
7페이지 | 1,500원 | 2013.12.23
압력 P는 P=x1P10+x2P20=x1P10-P20+P20이 되어 x1의 일차함수로 나타낼 수 있다. 실제용액에서 각 성분의 활동상수를 1이라고 가정하면 y1P와 y2P는 각각 x1P1과 x2P2로 쓸 수 있다. 즉 일정한 온도에서 혼합용액 속의 각 성분의 분압은 혼합물의 몰분율에 비례한다. 이를 라울의 법칙이라고 한다. 하지만 대부분
12페이지 | 2,000원 | 2013.12.23





 영역
영역 







