일반화학실험 - 일정 성분비의 법칙
 등록일 / 수정일
등록일 / 수정일 페이지 / 형식
페이지 / 형식 자료평가
자료평가 구매가격
구매가격
- 2013.12.23 / 2019.12.24
- 5페이지 /
 hwp (아래아한글2002)
hwp (아래아한글2002) - 평가한 분이 없습니다. (구매금액의 3%지급)
- 1,200원
최대 20페이지까지 미리보기 서비스를 제공합니다.
자료평가하면 구매금액의 3%지급!
 1
1 2
2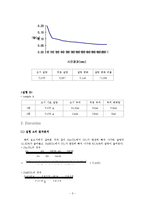 3
3 4
4 5
5
추천 연관자료
- 본문내용
-
1. Abstract
원자는 물질세계의 기본 단위이다.① 우리 주변의 많은 물질들은 바로 이 원자들의 결합으로 이루어져 있다. 원자들이 다양하게 결합하여서 수많은 물질을 이루는 것이다.
그러나 이 원자들 간의 결합에는 일정한 규칙이 있는데, 그 중에서 대표적인 것이 일정성분비의 법칙(law of definite proportions)이다. 일정성분비의 법칙은 1799년 J.L.Proust에 의해서 발견된 것으로 화합물을 구성하는 각 성분원소의 질량의 비는 일정하다는 법칙이다.② 특정한 화합물은 특정한 성분비를 가지기 때문에 질량과 부피를 분석하여 모르는 화합물의 원자비를 알아내면 실험식(또는 분자식)을 알아낼 수 있고, 화합물을 추정할 수 있다.
오늘 실험에서는 Na2CO3와 NaHCO3의 질량변화와 부피변화를 관찰해서 시료를 추정해 본다. 주변 환경과 실험기구 때문에 오차가 많이 났다.
- 참고문헌
-
① http://147.46.41.146/~chemlab/exp/exp2.htm 참조
② http://100.naver.com/100.php?where=100&id=136174 참조
자료평가
-
아직 평가한 내용이 없습니다.
오늘 본 자료
더보기

최근 판매 자료
- 바이오인포매틱스(생물정보학)개념, 바이오인포매틱스(생물정보학)정보과학적기법, 바이오인포매틱스(생물정보학)현황, 바이오인포매틱스 과제
- [생물학] 유전자와 돌연변이
- 디지털 회로 실험 및 설계 - ADC(Analog to Digital Converter) 실험 1
- 회로이론1 이정훈 년도 표기
- 회로이론1 이정훈 년도 표기 X
- 연세대 고려대 성균관대 한양대 기계공학 대학원 구술면접자료 및 공부
- 전자기학 응용예제_04장 hayt
- [생화학 실험] TLC를 이용한 아미노산의 적정실험
- 광결정(Photonic crystal)
- 광물의 굳기와 조흔색 - 5E모형(중학교 1학년 과학 파트 수업 지도안)
저작권 관련 사항 정보 및 게시물 내용의 진실성에 대하여 레포트샵은 보증하지 아니하며, 해당 정보 및 게시물의 저작권과 기타 법적 책임은 자료 등록자에게 있습니다. 위 정보 및 게시물 내용의 불법적 이용, 무단 전재·배포는 금지됩니다. 저작권침해, 명예훼손 등 분쟁요소 발견시 고객센터에 신고해 주시기 바랍니다.









