[화학공학실험] 기액평형
 등록일 / 수정일
등록일 / 수정일 페이지 / 형식
페이지 / 형식 자료평가
자료평가 구매가격
구매가격
- 2011.11.17 / 2019.12.24
- 13페이지 /
 hwp (아래아한글2002)
hwp (아래아한글2002) 



 1건 (구매금액의 3%지급)
1건 (구매금액의 3%지급)- 1,400원
최대 20페이지까지 미리보기 서비스를 제공합니다.
자료평가하면 구매금액의 3%지급!
 1
1 2
2 3
3 4
4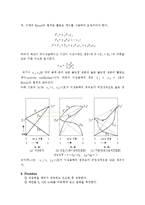 5
5 6
6 7
7 8
8 9
9 10
10 11
11 12
12 13
13- 목차
-
목 차
1. Title : 기-액 평형
2. Date :
3. Section & Name :
4. Object
5. Theory
① 평형의 정의와 평형조건
② 기-액평형(vapor-liquid equilibrium)
③ 단증류(simple distillation)
④ Raoult의 법칙
⑤ Henry의 법칙
⑥ 증기압곡선과 휘발도
6. Procedure
7. Reagent & Apparatus
8. Data & Result
1) 검량선 작성
2) 기-액 평형 실험
3) data 분석
9. Discussion
10. Reference
- 본문내용
-
(3.2)
식(3.2)에서 보면 희박용액에 대하여 농도 C2는 용해된 물질의 몰 분율에 비례한다.
식(3.2)이 Henry의 법칙으로 자주 이용된다.
⑥ 증기압곡선과 휘발도
- Raoult의 법칙에 따르는 이상용액은 용약을 구성하는 분자들 간의 인력이 비슷한 경우로써 벤젠-톨루엔 계, 메탄올-에탄올 계 등이 이에 해당 한다 . 이 경우 일정한 온도에서의 증기압 곡선은 아래 그림의 (a)와 같다.
그러나 실제 용액의 경우는 Raoult의 법칙으로부터 벗어나는데, (b)와 같이 이상용액에 비해 증기압이 크게 나타나는 겨우를 정편차라고 하며, 증기압 곡선은 극대점 Ah를 갖는다. 예를 들어 물-에탄올 계, 에탄올-벤젠 계 및 아세톤-CS2와 같이 동종분자 간 인력보다 클 대 나타난다. 반면 (c)은 증기압이 이상용액에 비해 작게 나타나는 경우로써 부편차라고 하며, 극소점 Al를 갖는다. 아세톤-클로로포름 계, 물-염산 계, 물-질산, 물-황산 계와 같이 동종분자 간 인력이 이종분자간 인력보다 작을 대 이러한 현상이 일어난다. 이러한 용약을 비이상용액(nonideal solution)이라고 하며, 이때의 Raoult의 법칙은 활동도 계수를 사용하여 보정되어야 한다.
따라서 액상이 비이상용액이고 기상이 이상기체인 경우(즉 P = PA + PB )의 비휘발도는 다음 식으로 표시된다.
여기서 ,는 각각 용액 중의 낮은 끓는점 성분과 높은 끓는점 성분의 활동도계수(activity coefficient)이다. 따라서 이상용액의 경우 = = 1로써 Raoult의 법칙과 같아진다.
아래 그림의 (b)는 >1, >1로써 이상용액의 경우보다 비정상적으로 높은 경우이며(c)는 <1, <1로써 이상용액의 경우보다 비정상적으로 낮은 경우이다.
- 참고문헌
-
10. Reference
① 단위조작 입문/ 박창호, 김우식, 정인식/ 지인당/2001.3.5/ 175p~186p
② 단위조작 실험/ 고완석, 심현호/ 학연사/ 2003.2.20/165p~168p
③ 화학공학실험/ 성기천, 이진회, 김기준/ 사이텍미디어/ 2000/ 445p~457p
자료평가





- 잘정리되어 있음 보기가편함
- lar***
(2014.11.09 14:48:40)
오늘 본 자료
더보기

최근 판매 자료
- 모발 염색의 종류와 원리
- [조경실무]조경실무 - 도시경관의 문제점과 발전방향
- 바이오인포매틱스(생물정보학)개념, 바이오인포매틱스(생물정보학)정보과학적기법, 바이오인포매틱스(생물정보학)현황, 바이오인포매틱스 과제
- [생물학] 유전자와 돌연변이
- 디지털 회로 실험 및 설계 - ADC(Analog to Digital Converter) 실험 1
- 회로이론1 이정훈 년도 표기
- 회로이론1 이정훈 년도 표기 X
- 연세대 고려대 성균관대 한양대 기계공학 대학원 구술면접자료 및 공부
- 전자기학 응용예제_04장 hayt
- [생화학 실험] TLC를 이용한 아미노산의 적정실험
저작권 관련 사항 정보 및 게시물 내용의 진실성에 대하여 레포트샵은 보증하지 아니하며, 해당 정보 및 게시물의 저작권과 기타 법적 책임은 자료 등록자에게 있습니다. 위 정보 및 게시물 내용의 불법적 이용, 무단 전재·배포는 금지됩니다. 저작권침해, 명예훼손 등 분쟁요소 발견시 고객센터에 신고해 주시기 바랍니다.









