실험보고서 - 산, 염기 적정을 통해 적정곡선을 얻어 해석하는 방법, 이온화 상수 결정
 등록일 / 수정일
등록일 / 수정일 페이지 / 형식
페이지 / 형식 자료평가
자료평가 구매가격
구매가격
- 2013.12.23 / 2019.12.24
- 5페이지 /
 hwp (아래아한글2002)
hwp (아래아한글2002) - 평가한 분이 없습니다. (구매금액의 3%지급)
- 1,500원
최대 20페이지까지 미리보기 서비스를 제공합니다.
자료평가하면 구매금액의 3%지급!
 1
1 2
2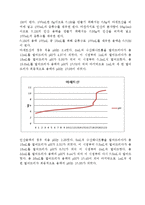 3
3 4
4 5
5
추천 연관자료
- 하고 싶은 말
- 본문내용
-
1. 서론(Introduction)
○ 실험 목적
pH메타를 이용한 산 염기 적정을 통해 적정곡선을 얻어 이해하고 해석한다. 이를 이용해 이온화 상수를 결정하고 산의 세기와 종류에 따라 변화하는 적정곡선을 확인한다.
○ 실험 이론
화학평형 : 반대 방응이 서로 같은 속도로 진행될 때를 이르는 말. 반응물로부터 생성물이 생성되는 속도와 생성물로부터 반응물이 생성되는 속도가 같아 마치 반응이 정지한 것처럼 보인다.
평형혼합물은 반응이 가역적이기 때문에 얻어진다.
A ↔ B
A가 분해해서 B를 생성하는 정반응과 B로부터 A를 다시 생성하는 역반응을 생각해보면 정반응과 역반응은 둘 다 단일단계 반응이다.
정반응 : A→B 속도f = kf[A]
역반응 : B→A 속도r = kr[B]
여기서 kf와 kr은 각각 정반응과 역반응의 속도 상수 이다. 평형에서 반응물로부터 생성물이 생성되는 속도는 생성물로부터 반응물이 생성되는 속도와 같다.
[B]2/[A]2 = kf/kr = 평형상수
- 참고문헌
-
5. 참고 문헌
참고 1 : Brown LeMay Bursten "일반화학“ 10th ed. p596 녹문당(2007)
참고 2 : ATKINS JONES “화학의원리“ 4th ed. p469 자유아카데미(2008)
참고 3 : 크레이그 크리들 “세상에서 가장 재미있는 화학” p164 궁리(2008)
참고 4 : Raymond Chang “일반화학“ 8th ed. p664 자유아카데미(2006)
자료평가
-
아직 평가한 내용이 없습니다.
오늘 본 자료
더보기

최근 판매 자료
- 물리화학 보고서- Conjugation 염료의 흡수 스펙트럼
- 일반물리학 실험 - 일과 에너지 결과보고서
- 디지털 회로 실험 및 설계 - ADC(Analog to Digital Converter) 실험 1
- [도로교통] 도로 폭에 따른 구간 내 LOS 분석
- [나노기술]나노기술의 정의와 응용분야 및 발전방향(A+레포트)★★★★★
- [도로교통] 도로 폭에 따른 구간 내 LOS 분석
- [창의공학] 계단 오르는 유모차 문제점 및 해결방안
- 모발 염색의 종류와 원리
- [조경실무]조경실무 - 도시경관의 문제점과 발전방향
- 바이오인포매틱스(생물정보학)개념, 바이오인포매틱스(생물정보학)정보과학적기법, 바이오인포매틱스(생물정보학)현황, 바이오인포매틱스 과제
저작권 관련 사항 정보 및 게시물 내용의 진실성에 대하여 레포트샵은 보증하지 아니하며, 해당 정보 및 게시물의 저작권과 기타 법적 책임은 자료 등록자에게 있습니다. 위 정보 및 게시물 내용의 불법적 이용, 무단 전재·배포는 금지됩니다. 저작권침해, 명예훼손 등 분쟁요소 발견시 고객센터에 신고해 주시기 바랍니다.









