[물리화학실험]전기전도도 측정
 등록일 / 수정일
등록일 / 수정일 페이지 / 형식
페이지 / 형식 자료평가
자료평가 구매가격
구매가격
- 2010.04.01 / 2019.12.24
- 14페이지 /
 hwp (아래아한글2002)
hwp (아래아한글2002) - 평가한 분이 없습니다. (구매금액의 3%지급)
- 2,000원
최대 20페이지까지 미리보기 서비스를 제공합니다.
자료평가하면 구매금액의 3%지급!
 1
1 2
2 3
3 4
4 5
5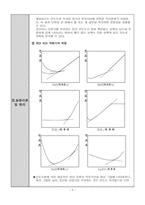 6
6 7
7 8
8 9
9 10
10 11
11 12
12 13
13 14
14
추천 연관자료
- 하고 싶은 말
-
[물리화학실험]전기전도도 측정 실험 레포트 입니다.
강전해질과 약전해질의 전기전도를 측정하여 이론치와 비교한 레포트입니다.
전도도 뿐만 아니라 저항도, 비전도도, 당량전도도로 함께 측정하였습니다.
계산 과정을 생략하지 않고 상세히 기록했습니다.
실험 결과를 그래프로 표현하였습니다.
- 목차
-
Ⅰ.실험목적
Ⅱ.실험기구 및 시약
Ⅲ.실험이론 및 원리
Ⅳ.실험과정
실험결과
참고문헌
- 본문내용
-
(1)실험기구
① 비커(50ml) ② 메스플라스크(250ml) ③ 화학저울 ④ 전기전도도미터
(2)실험시약
① NaCl(염화나트륨)
▶등축정계에 속하는 무색 결정으로, 결정 속에서 결합간격 2.82 , 녹는점 800.4℃, 끓는점1,400℃, 비중 2.16(20 ℃), 굴절률 1.5443이다. 녹는점 이 상에서는 휘발성이 높고, 기체가 되면 NaCl 분자가 존재한다. 보통 마그네 슘 등의 염류를 함유하며 조해성이 있다. 100g의 물에 0℃에서 35.7g, 100℃ 에서 39.8g 녹는다.
알코올에는 잘 녹지 않으며, 포화용액은 0℃ 이하에서 무색 단사정계의 이 수화물 NaCl·2H2O를 생성하며, -21.3℃에서 함빙정(含氷晶)을 만든다. 이것을 이용하여, 염화나트륨과 분쇄한 얼음을 섞음으로써 -21℃의 냉각제 를 만들기도 한다.
② NaOH(수산화나트륨)
▶수산화나트륨의 화학식은 NaOH이다. 순수한 것은 무색의 투명한 결정이지 만, 보통은 약간 불투명한 흰색 고체다. 탄산나트륨 등의 불순물을 함유하고 있다. 상온에서는 사방정계(斜方晶系)이다. 완전히 탈수시킨 수산화나트륨의 녹는점은 328℃이지만, 보통은 약간의 수분이 들어 있어 318.4℃이다. 끓는 점 1,390℃, 비중 2.13이다.
조해성(潮解性)이 강하여 공기중에 방치하면, 습기와 이산화탄소를 흡수한 다. 그러면 탄산나트륨이 되어, 결정을 석출한다. 물에 잘 녹으며, 그때 다량 의 열을 발생한다. 수용액은 강한 알칼리성이며, 용해도는 물 100g에 대하 여 0℃에서 42g, 100℃에서 347g이다. 알코올이나 글리세롤에는 잘 녹지 만, 에테르나 아세톤에는 녹지 않는다. 강하게 가열해도 산화물과 물로 분해 하지 않는다. 그러나 쉽게 융해하여 금·백금·규산 등을 침식하므로, 융해 수산화나트륨은 은·니켈 등의 용기를 써서 취급해야 한다.
- 참고문헌
-
◆ 물리화학, P.W Atkins 8/E
◆ 물리화학, Raymond Chang 1999
◆ 물리화학실험, 대한학회지 2002
◆ 물리화학 실험, Salzberg, H. W(형설출판사)
◆ 네이버 백과사전
자료평가
-
아직 평가한 내용이 없습니다.










