[화학공학실험] 기-액 결과
 등록일 / 수정일
등록일 / 수정일 페이지 / 형식
페이지 / 형식 자료평가
자료평가 구매가격
구매가격
- 2010.08.07 / 2019.12.24
- 6페이지 /
 hwp (아래아한글2002)
hwp (아래아한글2002) - 평가한 분이 없습니다. (구매금액의 3%지급)
- 1,100원
최대 20페이지까지 미리보기 서비스를 제공합니다.
자료평가하면 구매금액의 3%지급!
 1
1 2
2 3
3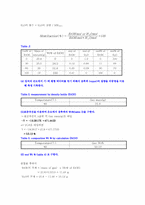 4
4 5
5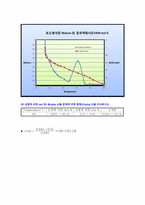 6
6
추천 연관자료
- 목차
-
2. 실험결과
(1) Table .1 Water EtOH Standard Curve
(2) 표준곡선을 구한다.
(3) boiler 안의 mixture의 조성(mol%)을 구한다.
(4) 임의의 온도에서 기-액 평형 데이터를 얻기 위해서 응축액 (vapor)의 질량을 비중병을 이용해 측정 기록한다.
(5)표준곡선을 이용하여 온도에서 응축액의 Wt%(table 3)을 구한다.
(6) mol Wt % (table 4) 로 구한다.
(7)다음의 평형도 (Table. 5 )를 이용하여 온도에 따른 mixture 와 응축액에서 EtOH mol%를 그래프로 나타내시오.
(8) 실험에 의한 mol Wt %(table 4)를 문헌에 의한 평형도(table 5)를 비교하시오.
- 본문내용
-
엑셀 데이터 회귀 분석에 의해 A, B 값을 구해보면
A = -19.3817 , B = 471.4423 이라는 값을 얻게 되며
결정계수 이라는 값을 얻게 되어 비교적 1에 가까운 결정계수를 얻는다. 따라서 최종적으로,
[Y = -19.3817X +471.4423]
이라는 식을 얻을 수 있다.
(3) boiler 안의 mixture의 조성(mol%)을 구한다.
MWEtOH = 46.07 g/mol, MWH2O = 18.02 g/mol
EtOH 질량 = Mass of mixture × Wt% of EtOH
H2O의 질량 = Mass of mixture - EtOH 질량
EtOH의 몰수 = EtOH 질량 / MWEtOH
H2O의 몰수 = H2O의 질량 / MWH2O
Table .2
Vol% of
EtOH
Mass of mixture(g)
Wt% of EtOH
mol of
EtOH
mol of
H2O
mol% of
EtOH
mol% of
H2O
0
23.9
0
0
1.3
0
100
30
23.3
24.5
0.12
0.98
11
89
60
22
51.8
0.25
0.59
30
70
100
19
100
0.41
0
100
0
(4) 임의의 온도에서 기-액 평형 데이터를 얻기 위해서 응축액 (vapor)의 질량을 비중병을 이용해 측정 기록한다.
Table 2. measurement by density bottle (EtOH)
Temperature(℃)
Gas mass(g)
80
21.6
(5)표준곡선을 이용하여 온도에서 응축액의 Wt%(table 3)을 구한다.
→ 표준곡선의 x값에 각 Gas mass(g)을 대입
자료평가
-
아직 평가한 내용이 없습니다.
오늘 본 자료
더보기

최근 판매 자료
- 물리화학 보고서- Conjugation 염료의 흡수 스펙트럼
- 일반물리학 실험 - 일과 에너지 결과보고서
- 디지털 회로 실험 및 설계 - ADC(Analog to Digital Converter) 실험 1
- [도로교통] 도로 폭에 따른 구간 내 LOS 분석
- [나노기술]나노기술의 정의와 응용분야 및 발전방향(A+레포트)★★★★★
- [도로교통] 도로 폭에 따른 구간 내 LOS 분석
- [창의공학] 계단 오르는 유모차 문제점 및 해결방안
- 모발 염색의 종류와 원리
- [조경실무]조경실무 - 도시경관의 문제점과 발전방향
- 바이오인포매틱스(생물정보학)개념, 바이오인포매틱스(생물정보학)정보과학적기법, 바이오인포매틱스(생물정보학)현황, 바이오인포매틱스 과제
저작권 관련 사항 정보 및 게시물 내용의 진실성에 대하여 레포트샵은 보증하지 아니하며, 해당 정보 및 게시물의 저작권과 기타 법적 책임은 자료 등록자에게 있습니다. 위 정보 및 게시물 내용의 불법적 이용, 무단 전재·배포는 금지됩니다. 저작권침해, 명예훼손 등 분쟁요소 발견시 고객센터에 신고해 주시기 바랍니다.









