화학반응속도 보고서
 등록일 / 수정일
등록일 / 수정일 페이지 / 형식
페이지 / 형식 자료평가
자료평가 구매가격
구매가격
- 2009.07.23 / 2019.12.24
- 12페이지 /
 hwp (아래아한글2002)
hwp (아래아한글2002) - 평가한 분이 없습니다. (구매금액의 3%지급)
- 1,400원
최대 20페이지까지 미리보기 서비스를 제공합니다.
자료평가하면 구매금액의 3%지급!
 1
1 2
2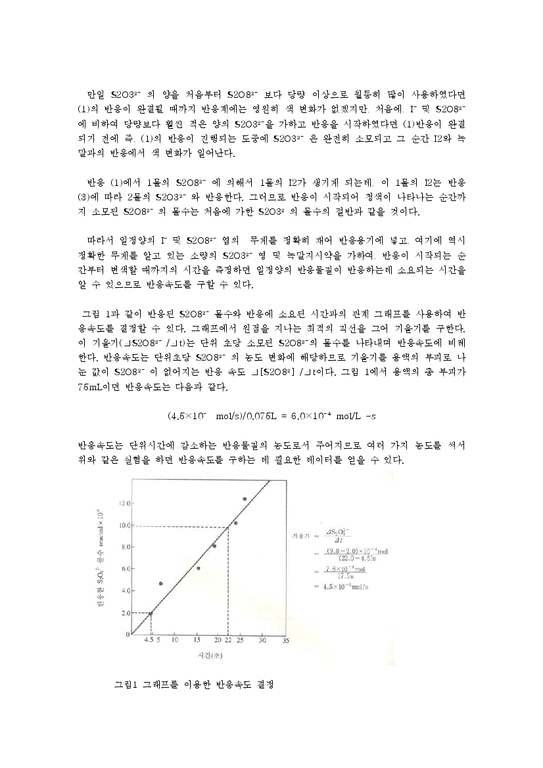 3
3 4
4 5
5 6
6 7
7 8
8 9
9 10
10 11
11 12
12
추천 연관자료
- 목차
-
1. 실험 목적
2. 이론
1) 시계 반응
2) 반응속도식 / 반응속도상수 / 반응차수
3. 실험 기구 및 시약
4. 실험 방법
5. 실험 결과
1. 반응차수 및 속도상수의 결정
2. 최종 반응 속도식
3. 농도 변화에 따른 반응속도의 변화
1) I- 이온이 일정할 때 S2O8²¯ 이온 농도의 변화에 따른 반응속도 변화
2) S2O8²¯ 이온이 일정할 때 I- 이온 농도의 변화에 따른 반응속도 변화
4. 촉매의 영향
5. 고찰
6. 참고문헌
- 본문내용
-
화학 반응 속도
1. 실험 목적
화학반응속도는 농도, 온도 및 촉매의 영향을 받는다. 농도 변화에 따른 반응속도를 측정함으로써 반응속도상수와 반응차수를 결정할 수 있다. 일 실험에서는 소위 시계반응을 이용하여 2I¯ + S2O8²¯ → I2 + 2SO4²¯ 반응의 속도에 미치는 농도의 영향을 조사하고, 반응속도상수 및 반응차수 구하는 방법을 습득한다.
2. 이론
1) 시계 반응
이 실험에서는 화학반응속도에 미치는 농도의 영향을 조사하는 것이 목적이다. 다음과 같은 요오드화 이온과 과산화이황산 이온의 반응을 조사하여 보자.
I¯ + S2O8²¯ → I2 + 2SO4²¯
(1)
이 반응은 실온에서는 상당히 느리게 진행되는데, 그 반응속도는 다음 식으로 나타낼 수 있다.
반응속도=k[I¯][S2O8²¯]ⁿ
(2)
여기서 k는 반응속도상수이며, m과 n은 반응차수로서 0, 1, 2, 3과 같은 정수이다. 이온의 농도는 mol/L로 나타낸다. 반응속도는 식 (2)에서 알 수 있듯이 반응물의 농도에 따라서 영향을 받는다. 또한 반응속도는 온도와 촉매의 영향을 받는다. 그러나 이 실험에서는 반응속도에 미치는 농도의 영향만을 조사하기로 한다.
이 실험의 주목적은 속도상수 k의 값과 반응차수 m과 n을 구하는 것이다. 우리들이 반응속도를 측정하려는 방법은 소위 시계반응이라 부르는 반응인데, 이것은 한 반응의 종말점을 자동적으로 알 수 있는 반응이다. 우리가 조사대상으로 하고 있는 반응 (1)을 녹말 존재하에서 다음의 반응 (3)과 동일 용기내에서 동시에 일어나도록 한다.
I2 + 2S2O3²¯ → 2I¯ + S4O6²¯
(3)
반응 (3)응 반응 (1)에 비하여 훨씬 빨리 진행된다. 그러므로 반응 (1)에서 생성된 I2분자는 같은 반응요기에 들어 있던 S2O3²¯ 이온과 재빨리 반응하여 없어지게 되어 S2O3²¯ 이온이 완전히 소모되지 않는 한 I2의 농도는 영이다. 반응이 진행되어 S2O3²¯ 이온이 모두 소모되면 반응 (1)만이 일어나므로 I2 분자가 용액 속에 남게 되고, I2 분자가 생성되는 순간 이것이 녹말과 반응하여 청색을 띠게 되어 일정량의 S2O3²¯ 이온이 모두 반응하여 없어지는데 필요한 시간을 알려주므로 시계와 같은 구실을 한다.
만일 S2O3²¯ 의 양을 처음부터 S2O8²¯ 보다 당량 이상으로 월등히 많이 사용하였다면 (1)의 반응이 완결될 때까지 반응계에는 영원히 색 변화가 없겠지만, 처음에, I¯ 및 S2O8²¯ 에 비하여 당량보다 훨씬 적은 양의 S2O3²¯을 가하고 반응을 시작하였다면 (1)반응이 완결되기 전에 즉, (1)의 반응이 진행되는 도중에 S2O3²¯ 은 완전히 소모되고 그 순간 I2와 녹말과의 반응에서 색 변화가 일어난다.
반응 (1)에서 1몰의 S2O8²¯ 에 의해서 1몰의 I2가 생기게 되는데, 이 1몰의 I2는 반응 (3)에 따라 2몰의 S2O3²¯ 와 반응한다. 그러므로 반응이 시작되어 청색이 나타나는 순간까지 소모된 S2O8²¯ 의 몰수는 처음에 가한 S2O3² 의 몰수의 절반과 같을 것이다.
따라서 일정양의 I¯ 및 S2O8²¯ 염의 무게를 정확히 재어 반응용기에 넣고, 여기에 역시 정확한 무게를 알고 있는 소량의 S2O3²¯ 영 및 녹말지시약을 가하여, 반응이 시작되는 순간부터 변색할 때까지의 시간을 측정하면 일정양의 반응물질이 반응하는데 소요되는 시간을 알 수 있으므로 반응속도를 구할 수 있다.
그림 1과 같이 반응된 S2O8²¯ 몰수와 반응에 소요된 시간과의 관계 그래프를 사용하여 반응속도를 결정할 수 있다. 그래프에서 원점을 지나는 최적의 직선을 그어 기울기를 구한다. 이 기울기(⊿S2O8²¯/⊿t)는 단위 초당 소모된 S2O8²¯의 몰수를 나타내며 반응속도에 비례한다. 반응속도는 단위초당 S2O8²¯ 의 농도 변화에 해당하므로 기울기를 용액의 부피로 나눈 값이 S2O8²¯ 이 없어지는 반응 속도 ⊿[S2O8²]/⊿t이다. 그림 1에서 용액의 총 부피가 75mL이면 반응속도는 다음과 같다.
(4.5×10¯ mol/s)/0.075L = 6.0×10¯⁴mol/L -s
반응속도는 단위시간에 감소하는 반응물질의 농도로서 주어지므로 여러 가지 농도를 써서
- 참고문헌
-
대한 화학외, 표준일반화학 실험, 제5판, 천문각, 1999
일반화학교재 연구회, 일반화학, 천문각
Brown LeMay Bursten, “일반화학 제7판”, 녹문당
화학교재편찬위원회, 화학의 세계, 지샘, 1999
Raymond Chang, "일반화학 제7판“, 자유아카데미, 2006
나춘기 외 3명, 공업물리화학, chap7, 1999
이갑상, 일반화학실험, 대학서림, 2002 : p179~184
하이탑 고등학교 화학2 : p54~56, 77~82
http://100.naver.com/100.nhn?docid=147530
http://blog.naver.com/whitoak?Redirect=Log&logNo=18727985
http://100.naver.com/100.nhn?docid=173476
자료평가
-
아직 평가한 내용이 없습니다.
오늘 본 자료
더보기

최근 판매 자료
- 기초전자실험 with PSpice 최대전력 전달조건 레포트
- 물리화학 보고서- Conjugation 염료의 흡수 스펙트럼
- 일반물리학 실험 - 일과 에너지 결과보고서
- 디지털 회로 실험 및 설계 - ADC(Analog to Digital Converter) 실험 1
- [도로교통] 도로 폭에 따른 구간 내 LOS 분석
- [나노기술]나노기술의 정의와 응용분야 및 발전방향(A+레포트)★★★★★
- [도로교통] 도로 폭에 따른 구간 내 LOS 분석
- [창의공학] 계단 오르는 유모차 문제점 및 해결방안
- 모발 염색의 종류와 원리
- [조경실무]조경실무 - 도시경관의 문제점과 발전방향
저작권 관련 사항 정보 및 게시물 내용의 진실성에 대하여 레포트샵은 보증하지 아니하며, 해당 정보 및 게시물의 저작권과 기타 법적 책임은 자료 등록자에게 있습니다. 위 정보 및 게시물 내용의 불법적 이용, 무단 전재·배포는 금지됩니다. 저작권침해, 명예훼손 등 분쟁요소 발견시 고객센터에 신고해 주시기 바랍니다.









