[화학실험] [물리화학실험]분몰랄 부피 측정(NaCl-H2O계)
 등록일 / 수정일
등록일 / 수정일 페이지 / 형식
페이지 / 형식 자료평가
자료평가 구매가격
구매가격
- 2007.06.01 / 2019.12.24
- 14페이지 /
 hwp (아래아한글2002)
hwp (아래아한글2002) 



 2건 (구매금액의 3%지급)
2건 (구매금액의 3%지급)- 1,500원
최대 20페이지까지 미리보기 서비스를 제공합니다.
자료평가하면 구매금액의 3%지급!
 1
1 2
2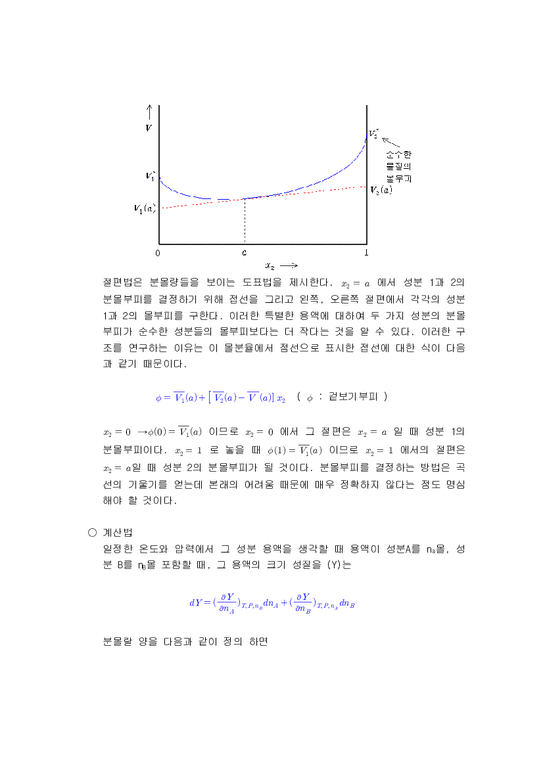 3
3 4
4 5
5 6
6 7
7 8
8 9
9 10
10 11
11 12
12 13
13 14
14
추천 연관자료
- 하고 싶은 말
-
한글의 수식기능은 텍스트로 변환이 되질 않기 때문에
위에 본문 내용에는 수식이 대부분 잘려있습니다.
그래도 파일 내용에는 전혀 이상이 없음을 알려드립니다.
- 목차
-
1. 제목
2. 실험일자
3. 실험목적
4. 이론적 배경
5. 시약 및 기구
6. 실험 방법
7. 결과 및 DATA 처리
8. 토의 및 고찰
9. 참고문헌
- 본문내용
-
1. 실험의 제목 : 분몰랄 부피 측정 ( NaCl-H2O계 )
2. 실험 일시 : 2005년 3월 31일 목요일
3. 실험 목적 : 조성률(무게를 퍼센트로 나타냄)을 미리 알고 있는 Nacl-H2O 용액 들 중에서 물과 소금의 분몰랄 부피를 결정한다.
4. 이론적 배경
분몰랄 성질은 고려되는 물질의 성질에 대해 물질 1mol의 기여를 나타낸다. 예를 들어, 그 성분 용액에서 어떤 한 용액의 부피가 충분히 커서 다른 성분을 1mol 가하여도 용액의 농도는 별로 변하지 않는다고 가정한다. 이때, 첨가한 성분 1mol당의 부피변화는 특정 압력, 온도 그리고 조서에서 특정한 값을 가지는데 이 것을 분몰랄 부피(partial molar volume)이라 한다. 그러므로 분몰랄 부피를 용 액의 그 성분 1mol에 해당하는 부피로 해석 할 수 있다.
다시 말해서 열린 계에서는 강도인자 (세기 성질: intensive state)인 P, T이외 에 물질이 드나들면 물질의 양(몰수)도 크기 인자 (크기 성질:extensive state) 영향을 주게 된다. (두 성질은 열역학 함수로 해결)
모든 크기 성질의 문볼랄(분몰 자유에너지, 분몰 엔탈피, 분몰 엔트로피 등의 총 명칭)중에서 가장 쉽게 이해하고 직접 측정할 수 있는 부피가 이용하기 쉽다.
○ 일정한 T, P에서 물질 의 몰을 혼합하여 용액을 만든 다고 가정하자. 을 T와 P에서 순물질 의 몰부피 라 하고 V*를 T와 P에서 혼합하지 않은 순수한 성분들의 전체 부피라 하자.
따라서
으로 나타낼 수 있다.
하지만 이들 각 성질들은 일반적으로 일정한 T와 P에서 성분들의 혼합에 따라 변하므로 이 성질들은 변수 T, P, n1, n2, … , nr에 의해 상태함수로 표현될 수 있다.
이 함수를 V에 관해 미분하면
-> 여기서 P, T는 일정하므로 dP,dT 값은 0 이다.
(처음 두 편도함수에 있는 첨자 ni는 모든 몰수가 일정하다는 의미한다. 첨자 ni≠j은 ni을 제외한 모든 몰수가 일정한 것을 나타낸다. 용액내 물질 j의 분몰 부피()는 I는 다음과 같이 정의된다.)
여기서 V는 용액의 부피이며, h함수는 T,P와 를 제외한 n를 제외한 모든 몰수 가 일정하다는 조건에서이다. 이 물질의 무한소량이 일정한 경우 P, T에서 용 액이 가해질 때 V의 변화라고 말할 수 있다. Euler의 정의에 따라서
이와 같이 용액의 체적은 혼합물 내의 물질들로 확인될 수 있는 분담 몫으로 이루어지지만 용액에서 물질의 분몰부피는 모든 화학종들의 농도에 의존한다 는 것을 주목해야 한다.
윗식을 용액의 전체량(몰 수)으로 나누면
여기서 는 용액의 몰부피이고 는 용액에서 물질의 의 몰분율이다.
이러한 더하기적 항은 최종용액의 조성에서 물질의 양과 물질의 분몰부피의 곱의 형태를 갖는다. 따라서 이 성분 용액에서
액체 용액의 분몰부피를 결정하기 위해 두가지 성분의 분몰부피와 몰분율의 함수로서 이 성분 용액의 몰부피 를 쓰면,
일정한 T와 P에서 이성분 용액의 몰부피는 다음과 같이 두 번째 성부의 몰분 율에 대해 그림을 그릴 수 있다.
절편법은 분몰량들을 보이는 도표법을 제시한다. 에서 성분 1과 2의 분몰부피를 결정하기 위해 접선을 그리고 왼쪽, 오른쪽 절편에서 각각의 성분 1과 2의 몰부피를 구한다. 이러한 특별한 용액에 대하여 두 가지 성분의 분몰 부피가 순수한 성분들의 몰부피보다는 더 작다는 것을 알 수 있다. 이러한 구 조를 연구하는 이유는 이 몰분율에서 점선으로 표시한 접선에 대한 식이 다음 과 같기 때문이다.
( : 겉보기부피 )
이므로 에서 그 절편은 일 때 성분 1의 분몰부피이다. 로 놓을 때 이므로 에서의 절편은 일 때 성분 2의 분몰부피가 될 것이다. 분몰부피를 결정하는 방법은 곡 선의 기울기를 얻는데 본래의 어려움 때문에 매우 정확하지 않다는 점도 명심 해야 할 것이다.
<중략>
- 참고문헌
-
물리화학실험(탐구당) p 72~80
물리화학실험(형설출판사) p 95~100
자료평가





- 이자료 받아봤는데 괜찮네요
- yspark***
(2010.12.23 18:41:48)





- 계산과정과 고찰내용이 충실해서 아주 만족했습니다.
- jeongs***
(2010.10.06 02:15:47)
오늘 본 자료
더보기

최근 판매 자료
- 물리화학 보고서- Conjugation 염료의 흡수 스펙트럼
- 일반물리학 실험 - 일과 에너지 결과보고서
- 디지털 회로 실험 및 설계 - ADC(Analog to Digital Converter) 실험 1
- [도로교통] 도로 폭에 따른 구간 내 LOS 분석
- [나노기술]나노기술의 정의와 응용분야 및 발전방향(A+레포트)★★★★★
- [도로교통] 도로 폭에 따른 구간 내 LOS 분석
- [창의공학] 계단 오르는 유모차 문제점 및 해결방안
- 모발 염색의 종류와 원리
- [조경실무]조경실무 - 도시경관의 문제점과 발전방향
- 바이오인포매틱스(생물정보학)개념, 바이오인포매틱스(생물정보학)정보과학적기법, 바이오인포매틱스(생물정보학)현황, 바이오인포매틱스 과제
저작권 관련 사항 정보 및 게시물 내용의 진실성에 대하여 레포트샵은 보증하지 아니하며, 해당 정보 및 게시물의 저작권과 기타 법적 책임은 자료 등록자에게 있습니다. 위 정보 및 게시물 내용의 불법적 이용, 무단 전재·배포는 금지됩니다. 저작권침해, 명예훼손 등 분쟁요소 발견시 고객센터에 신고해 주시기 바랍니다.









