생화학 1장~7장 레포트
 등록일 / 수정일
등록일 / 수정일 페이지 / 형식
페이지 / 형식 자료평가
자료평가 구매가격
구매가격
- 2010.03.31 / 2019.12.24
- 19페이지 /
 doc (MS워드 2003이하)
doc (MS워드 2003이하) - 평가한 분이 없습니다. (구매금액의 3%지급)
- 1,800원
최대 20페이지까지 미리보기 서비스를 제공합니다.
자료평가하면 구매금액의 3%지급!
 1
1 2
2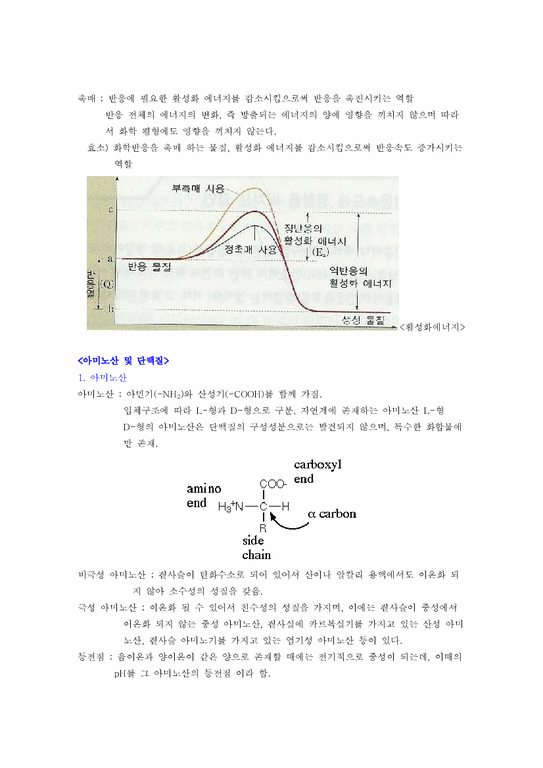 3
3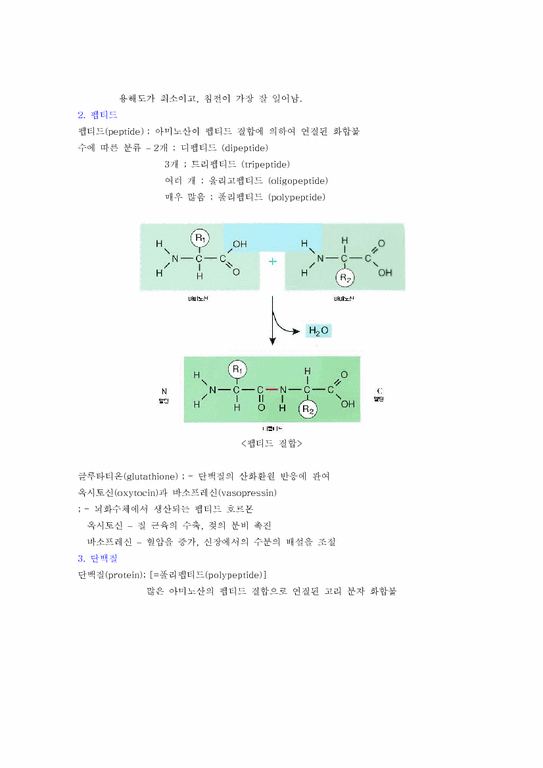 4
4 5
5 6
6 7
7 8
8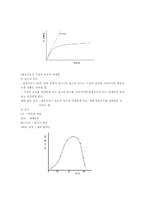 9
9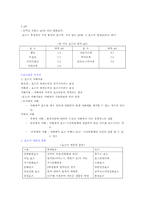 10
10 11
11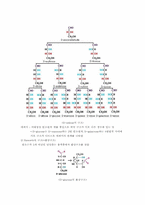 12
12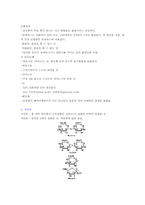 13
13 14
14 15
15 16
16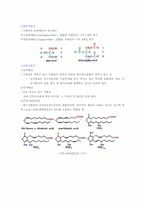 17
17 18
18 19
19
추천 연관자료
- 목차
-
<세 포>
1. 세포의 성질
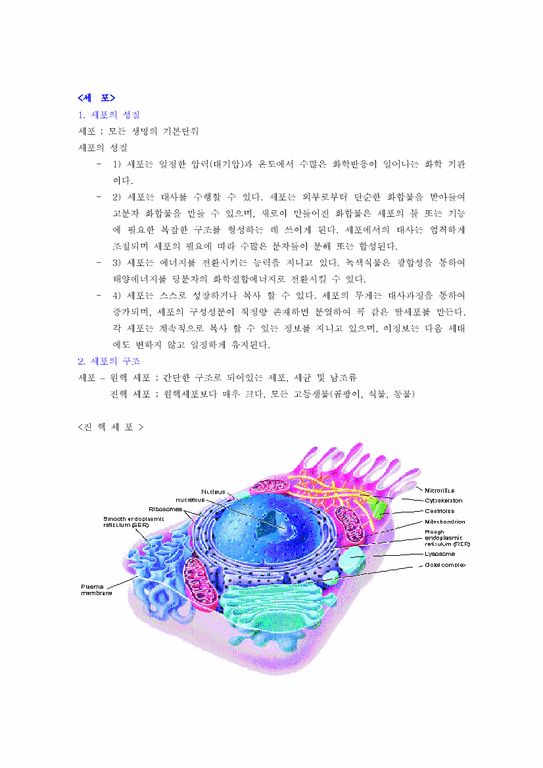
2. 세포의 구조
3. 세포의 성분
4. 세포반응의 특징
<아미노산 및 단백질>
1. 아미노산
2. 펩티드
3. 단백질
1) 단백질의 분류
2) 단백질 구조
3) 단백질의 입체구조
3. 단백질의 변성
<효 소>
1. 효소의 본체 및 기능
1) 효소반응의 특징
2) 효소작용의 기작
3) 효소의 보조인자
2. 효소반응에서 영향을 끼치는 인자
1)기질의 농도
2) 효소의 농도
3) 온도
4. pH
3.효소반응 속도론
1) 효소의 저해작용
4. 효소의 이름과 분류
<탄 수 화 물>
1. 단당류
1)단당류의 구조 및 입체이성질체
2) Haworth식 구조(=환상구조)
3)환원당
4) 당유도체
2. 이당류
1)maltose
2) cellobiose
3)lactose
3. 다당류
1)전분
2. 글리코겐(glycogen)
3. 셀룰로스
5. 점질다당류
6. 당단백질
7. 지방질당
<지 방 질>
1.지방산
2.중성지방질
3.복합지방질
1)인지방질
2)당지방질
3)프로스타글라딘
4. 스테로이드
5. 세포막
<대사의 개요>
1.분해 및 합성대사
2. 화학에너지와 역할
1)ATP의 역할
- 본문내용
-
2. 펩티드
펩티드(peptide) ; 아미노산이 펩티드 결합에 의하여 연결된 화합물
수에 따른 분류 – 2개 ; 디펩티드 (dipeptide)
3개 ; 트리펩티드 (tripeptide)
여러 개 ; 올리고펩티드 (oligopeptide)
매우 많음 ; 폴리펩티드 (polypeptide)
<펩티드 결합>
글루타티온(glutathione) ; - 단백질의 산화환원 반응에 관여
옥시토신(oxytocin)과 바소프레신(vasopressin)
; - 뇌화수체에서 생산되는 펩티드 호르몬
옥시토신 – 질 근육의 수축, 젖의 분비 촉진
바소프레신 – 혈압을 증가, 신장에서의 수분의 배설을 조절
3. 단백질
단백질(protein); [=폴리펩티드(polypeptide)]
많은 아미노산의 펩티드 결합으로 연결된 고리 분자 화합물
1) 단백질의 분류
구 분 단 백 질 보 기
조성에따른 분류
기능에 따른 분류
용해도에 따른 분류 단순단백질
복합단백질
유도단백질
수송단백질
저장단백질
수축운동단백질
구조단백질
방어단백질
조절단백질
효소단백질
물에 녹는 단백질
묽은 염용액에 녹는 단백질
알코올(80~90%)에 녹는 단백질
알칼리 용액에 녹는 단백질 알부민(혈청알부민)
글루텔린
글로불린
프롤라민
알부미노이드
핵단백질
인단백질
당단백질
지방단백질
금속단백질
색소단백질
변성단백질
분해단백질
헤모글로빈
글리아딘,오브알부민
악틴과 미오신
콜라겐, 젤라틴
항체
성장호르몬, 인슐린
소화효소
알부민
글로불린
프롤라민
글루텔린
* 분자 모양에 따라 – 구상단백질, 섬유상 단백질로도 나뉨.
2) 단백질 구조
수소결합(hydrogen bond)
; 수소가 전자를 끌어당기는 힘이 강한 산소나 질소와 공유결합을 하고 있는 경우에 수소나 이들 원자간에 약한 전기적 힘으로 이루어지는 결합
소수성 결합(hydrophobic interaction)
; 비극성아미노산의 곁사슬간에서 일어나며, 탄화수소로만 되어 있는 곁사슬을 가지고 있는 비극성 아미노산은 물에 잘 녹지 않는다. 이런 곁사슬을 소수성 그룹이라고 함.
소수성 효과 ; 소수성 아미노산끼리 단백질 안쪽으로 뭉치는 현상
단백질에는 많은 소수성아미노산이 있어 전체적인 소수성 효과는 단백질구조
를 유지하는데 중요한 역할을 함.
이온결합(ionic bond)
; 양전하와 음전하를 가진 이온간에 끌어당기는 힘을 말하며, 단백질을 구성하는 일부 아미노산의 곁사살은 중성에서 양전화와 음전화로 이온화 되므로 이온 결합을 할 수 있음.
이황화 결합(disulfide bond)
; 두 분자의 시스테인의 곁사슬 SH기 사이에서 형성되는 공유결합.
3) 단백질의 입체구조
1차 구조(primary structure) – 단백질의 아미노산 배열순서를 가리킴
2차 구조(secondary structure)
- 수소 결합에 의하여 이루어지는 것.
Ex) 나선구조; 펩티드 사슬이 단소에 있는 양쪽 결합에 회전하여 오른쪽으로 감긴 스프
링 모양으로 이루는 것
자료평가
-
아직 평가한 내용이 없습니다.
오늘 본 자료
더보기

최근 판매 자료
- 4차산업혁명이 우리사회에 미치는 영향분석과 정의,특징,기술분석 및 4차산업혁명에 대비한 우리의 자세
- 금속 조직실험레포트
- 지구온난화 양면성과 문제점 분석 및 우리나라 온난화 피해사례 연구 및 대책방안 제시 및 느낀점 - 지구온난화 문제연구
- 화학공학실험 - 활성탄을 이용한 아세트산 흡착량 계산(적정법)
- 화학 실험 - 질량측정과 액체 이동
- 심슨의 역설은 무엇인지(발생 원인 포함) 기술하고 우리 주위에서 발생한 사례를 찾아 요약 그 역설을 해결하여 올바로 해석
- 조명 디스플레이 - LED에 대해서
- [발광다이오드, LED, OLED, 플라스틱발광다이오드] 발광다이오드(LED)의 정의, 발광다이오드(LED)의 종류와 국내 발광다이오드(LED) 관련 사례 및 유기발광다이오드(OLED), 플라스틱발광다이오드(LED)에 관한 분석
- LED조명의 이해
- [열역학] 냉장고 증발기 시스템 열 효율성 고찰
저작권 관련 사항 정보 및 게시물 내용의 진실성에 대하여 레포트샵은 보증하지 아니하며, 해당 정보 및 게시물의 저작권과 기타 법적 책임은 자료 등록자에게 있습니다. 위 정보 및 게시물 내용의 불법적 이용, 무단 전재·배포는 금지됩니다. 저작권침해, 명예훼손 등 분쟁요소 발견시 고객센터에 신고해 주시기 바랍니다.









