회분식 반응기 레포트
 등록일 / 수정일
등록일 / 수정일 페이지 / 형식
페이지 / 형식 자료평가
자료평가 구매가격
구매가격
- 2010.01.09 / 2019.12.24
- 24페이지 /
 hwp (아래아한글2002)
hwp (아래아한글2002) 



 1건 (구매금액의 3%지급)
1건 (구매금액의 3%지급)- 1,500원
최대 20페이지까지 미리보기 서비스를 제공합니다.
자료평가하면 구매금액의 3%지급!
 1
1 2
2 3
3 4
4 5
5 6
6 7
7 8
8 9
9 10
10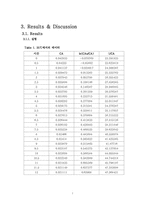 11
11 12
12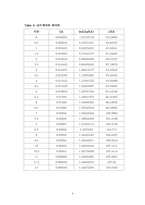 13
13 14
14 15
15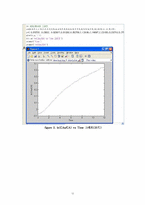 16
16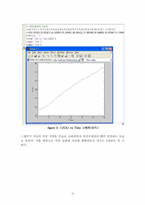 17
17 18
18 19
19 20
20
추천 연관자료
- 목차
-
Abstract
1.Introduction
1.1. 반응속도식
1.1.1. 반응 속도식의 정의
1.1.2. 반응차수
1.1.3. 반응 속도 상수
1.2. 회분식 반응기에 대한 해석
1.2.1.미분법
1.2.2.적분법
1.3. 회분식과 반회분식 반응기
1.4. 실험목적
2. Experiment
2.1. 실험 기구
2.2. 실험 방법
3. Results & Discussion
3.1. Results
3.1.1. 실험
3.2. Discussion
4. Conclusion
5. Reference
- 본문내용
-
Abstract
이 실험은 회분식 반응기를 사용하여 반응이 일어남에 따라 전도도와 pH가 변하는 실험을 통하여 반응 속도 상수와 반응차수를 알아보는 실험이었다. 반응기 내에서 에틸아세테이트와 NaOH를 반응시키는 것으로 분해되어있던 OH-기가 에틸아세테이트와 반응하여 에탄올이 만들어지는 화학반응이 일어난다. 또한 전도도와 pH가 감소하는 데이터를 얻고, 얻어진 데이터 처리를 하고 그래프를 그리는 것을 통해서 반응속도 상수와 반응차수를 알아내는 실험이었다. 실험은 회분식 반응기를 증류수로 세척하고, 세척한 회분식 반응기에 0.04M의 NaOH용액을 넣어주고 안정이 되면 에틸아세테이트를 5㎖를 넣어주어 교반하면서 전도도와 pH를 측정하였다. 온도가 25℃, 34℃, 45℃ 일 때 3번에 걸쳐서 실험을 하였다. 온도가 높아질수록 반응이 빨리 끝나서 전도도가 줄어들어 서서히 일정해지는 모습을 보이는 시간이 온도가 높을수록 짧아짐을 알 수 있었다. 또한 실험 결과를 분석해본 결과 반응차수는 2차임을 알 수 있었다. 이 실험에서는 온도에 따라 반응속도 상수가 낮아지다 다시 상승하는 모습을 보이고 있는데, 이론적으로는 온도에 따라 반응속도가 상승해야 하는 것과 비교하였을 때 실험에서 오차가 발생한 것을 알 수 있다. 오차 원인은 반응 속도 상수는 온도에 함수이므로 온도 조절을 잘해야 하는데, 반응기 내의 온도가 일정하게 유지되지 못하고 온도가 올라갔다 내려갔다가 하는 것을 보이면서 오차가 발생한 것으로 보였다. 또한 오차가 발생한 원인으로는 반응과정에서 완벽한 반응이 일어나지 않아서 오차가 발생하였을 가능성이 있다. 그리고 NaOH의 농도가 세척할 때 사용한 증류수가 조금이나마 남아있는 걸로 인해 묽어져서 오차가 발생하지 않았나 하는 생각이 들었다.
- 참고문헌
-
[1] 화학 공학 개론, 1st ed, 동화 기술, 고완석, 김영준, 임계규, 209-219
[2] 화학반응공학, 동화기술, 홍연기외 4명, 82-85
자료평가





- 회분식 반응기의 정의 같은게 필요했는데 하기 귀찮아서 받앗어요 ㅋㅋ
- dlarkd***
(2011.03.13 12:27:38)










