유기화학 실험 - nitration
 등록일 / 수정일
등록일 / 수정일 페이지 / 형식
페이지 / 형식 자료평가
자료평가 구매가격
구매가격
- 2009.11.08 / 2019.12.24
- 6페이지 /
 hwp (아래아한글2002)
hwp (아래아한글2002) - 평가한 분이 없습니다. (구매금액의 3%지급)
- 1,500원
최대 20페이지까지 미리보기 서비스를 제공합니다.
자료평가하면 구매금액의 3%지급!
 1
1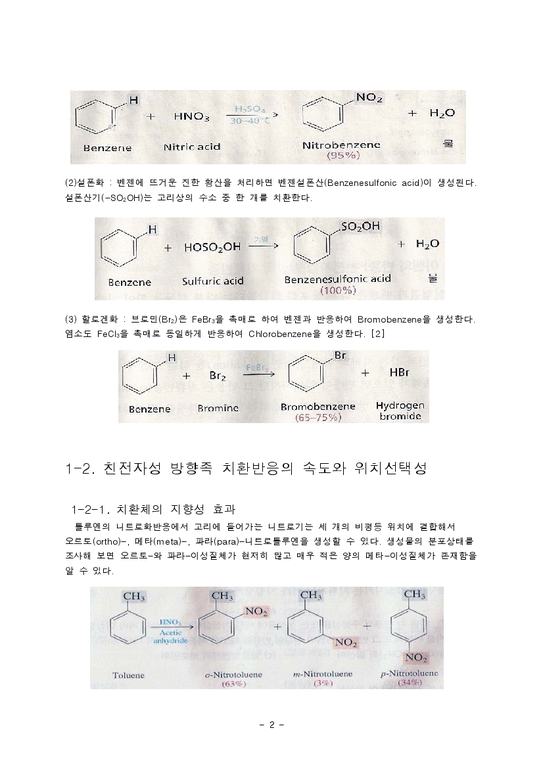 2
2 3
3 4
4 5
5 6
6
추천 연관자료
- 목차
-
[1. Introduction]
1-1. 친전자성 방향족 치환
1-1-1. 친전자성 방향족 치환의 메카니즘
1-1-2. 벤제의 대표적인 친전자성 방향족 치환반응
1-2. 친전자성 방향족 치환반응의 속도와 위치선택성
1-2-1. 치환체의 지향성 효과
1-3. 실험목적
[2. Experiment]
2-1. 실험재료
[3. Results]
3-1. Raw Data
3-2. Result Data
3-3. 고찰
[4. Conclusion]
[Reference]
- 본문내용
-
[1. Introduction]
1-1. 친전자성 방향족 치환
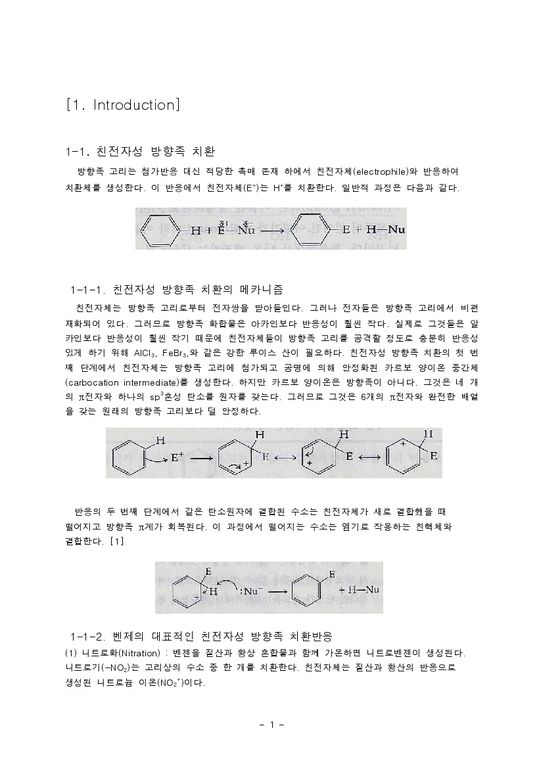
방향족 고리는 첨가반응 대신 적당한 촉매 존재 하에서 친전자체(electrophile)와 반응하여 치환체를 생성한다. 이 반응에서 친전자체(E+)는 H+를 치환한다. 일반적 과정은 다음과 같다.
1-1-1. 친전자성 방향족 치환의 메카니즘
친전자체는 방향족 고리로부터 전자쌍을 받아들인다. 그러나 전자들은 방향족 고리에서 비편재화되어 있다. 그러므로 방향족 화합물은 아카인보다 반응성이 훨씬 작다. 실제로 그것들은 알카인보다 반응성이 훨씬 작기 때문에 친전자체들이 방향족 고리를 공격할 정도로 충분히 반응성 있게 하기 위해 AlCl3, FeBr3,와 같은 강한 루이스 산이 필요하다. 친전자성 방향족 치환의 첫 번째 단계에서 친전자체는 방향족 고리에 첨가되고 공명에 의해 안정화된 카르보 양이온 중간체(carbocation intermediate)를 생성한다. 하지만 카르보 양이온은 방향족이 아니다. 그것은 네 개의 π전자와 하나의 sp3혼성 탄소를 원자를 갖는다. 그러므로 그것은 6개의 π전자와 완전한 배열을 갖는 원래의 방향족 고리보다 덜 안정하다.
반응의 두 번째 단계에서 같은 탄소원자에 결합된 수소는 친전자체가 새로 결합했을 때 떨어지고 방향족 π계가 회복된다. 이 과정에서 떨어지는 수소는 염기로 작용하는 친핵체와 결합한다. [1]
1-1-2. 벤제의 대표적인 친전자성 방향족 치환반응
(1) 니트로화(Nitration) : 벤젠을 질산과 황상 혼합물과 함께 가온하면 니트로벤젠이 생성된다. 니트로기(-NO2)는 고리상의 수소 중 한 개를 치환한다. 친전자체는 질산과 황산의 반응으로 생성된 니트로늄 이온(NO2+)이다.
(2)설폰화 : 벤젠에 뜨거운 진한 황산을 처리하면 벤젠설폰산(Benzenesulfonic acid)이 생성된다. 설폰산기(-SO2OH)는 고리상의 수소 중 한 개를 치환한다.
(3) 할로겐화 : 브로민(Br2)은 FeBr3을 촉매로 하여 벤젠과 반응하여 Bromobenzene을 생성한다. 염소도 FeCl3을 촉매로 동일하게 반응하여 Chlorobenzene을 생성한다. [2]
자료평가
-
아직 평가한 내용이 없습니다.
회원 추천자료
- [화학] 니트로벤젠의 합성
- Nitrobenzene 제조, m-Nitroanilin 제조 실험
- [광화학][광화학반응][광화학스모그][광화학산화제][철착화합물]광화학과 광화학반응, 광화학과 광화학스모그, 광화학과 광화학산화제, 광화학과 철착화합물 분석(광화학, 광화학반응, 광화학스모그, 광화학산화제)
- [산화][광화학산화제][항산화]산화와 광화학산화제, 산화와 항산화, 산화와 황산화, 산화와 인산화, 산화와 과산화물가, 산화와 일산화탄소, 산화와 금속산화막반도체전계효과트랜지스터, 산화와 산화전분 분석
- 방향족 화합물의 니트로화 반응 예비보고서
오늘 본 자료
더보기

최근 판매 자료
- 충북대_일반물리학및실험1_7주차_역학적에너지보존
- 전공면접, 전공 PT 면접 대비 - 기계공학과 전공 면접 기출 질문 모음(건설, 엔지니어링 등)
- [공학]토질공식
- 화학실험보고서 - 이산화탄소의 분자량
- 정보통신학개론_현재 스마트폰은 컴퓨터와 전화기의 기능이 융복합화된 IT기술의 총화라고 할 수 있습니다 본인이 가지고 있는 (관심있는) 스마트폰을 먼저 선정한 후 그 스마트폰의 사양과 특징 그리고 사용된 기술들에 대해 공부하고 조사정리한 내용을 제출하면 됩니다
- [일반화학실험보고서] 일반화학실험보고서-이산화탄소분자량
- 철근 인장강도 실험 결과 및 분석
- 토목지질학 - 암석의 분류에 대해서
- [일반물리학실험1] 운동량 보존 법칙
- 도시설계 정리 해설
저작권 관련 사항 정보 및 게시물 내용의 진실성에 대하여 레포트샵은 보증하지 아니하며, 해당 정보 및 게시물의 저작권과 기타 법적 책임은 자료 등록자에게 있습니다. 위 정보 및 게시물 내용의 불법적 이용, 무단 전재·배포는 금지됩니다. 저작권침해, 명예훼손 등 분쟁요소 발견시 고객센터에 신고해 주시기 바랍니다.









