[화학공학] 반응열 결과 & 나일론 예비
 등록일 / 수정일
등록일 / 수정일 페이지 / 형식
페이지 / 형식 자료평가
자료평가 구매가격
구매가격
- 2008.10.14 / 2019.12.24
- 8페이지 /
 hwp (아래아한글2002)
hwp (아래아한글2002) - 평가한 분이 없습니다. (구매금액의 3%지급)
- 1,400원
최대 20페이지까지 미리보기 서비스를 제공합니다.
자료평가하면 구매금액의 3%지급!
 1
1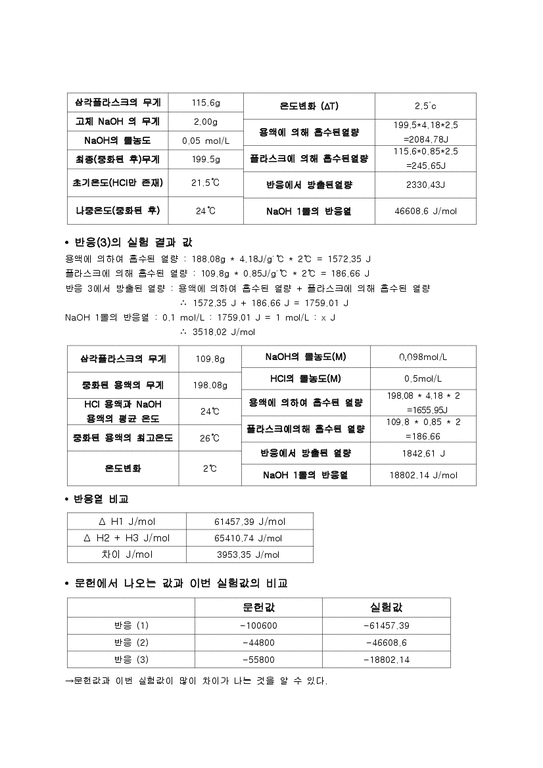 2
2 3
3 4
4 5
5 6
6 7
7 8
8
추천 연관자료
- 목차
-
결과보고서 - 반응열의 측정과 Hess의 법칙
■ 실험제목
■ 실험목적
■ 실험결과
■ 토의 및 고찰
예비보고서- 나일론 6,10 합성
■ 실험제목 : 나일론 6,10 합성
■ 실험목적
■ 이 론
■ 실험기구 & 시약
■ 실 험 방 법
■ 주 의 사 항
■ 참고 문헌
- 본문내용
-
■ 실험제목 : 반응열의 측정과 Hess의 법칙
실험일시
공동실험자
■ 실험목적
고체 수산화 나트륨과 염산의 중화반응을 한 단계 및 두 단계로 진행시켜 각 단계의
반응열을 측정하고, Hess의 법칙을 확인한다.
■ 실험결과
용액에 의한 온도변화는 q = m • S • ∆T로 구한다. 거기에 플라스크가 빼앗아간 열량을 더해주면 전체 반응열을 구할 수 있다. 물의 비열은 4.2J/K, 플라스크의 비열은 유리의 비열인 0.85J/K로 계산을 하였다
• 반응(1)의 반응열 측정
용액에 의하여 흡수된 열량 : 190.652g * 4.18J/g˙℃ * 3.5℃ = 2789.24 J
플라스크에 의해 흡수된 열량 : 109.8g * 0.85J/g˙℃ * 3.5℃ = 326.66 J
반응 1에서 방출된 열량 : 용액에 의하여 흡수된 열량 + 플라스크에 의해 흡수된 열량
∴ 2789.24J + 326.66J = 3115.89J
NaOH 1몰의 반응열 : 0.0507 mol/L : 3115.89 J = 1 mol/L : x J
∴ x = 61457.39 J/mol
삼각플라스크의 무게
109.8g
온도변화 (∆T)
3.5∘c
고체 NaOH 의 무게
2.03g
용액에 의해 흡수된열량
190.652*4.18*3.5 =2789.24J
NaOH의 몰농도
0.0507 mol/L
플라스크에 의해 흡수된열량
109.8*0.85*3.5 =326.66J
최종(중화된 후)무게
190.652g
초기온도(HCl만 존재)
22℃
반응에서 방출된열량
3115.89J
나중온도(중화된 후)
25.5℃
NaOH 1몰의 반응열
61457.39 J/mol
• 반응(2)의 실험 결과 값
용액에 의하여 흡수된 열량 : 199.5g * 4.18J/g˙℃ * 2.5℃ = 2084.78J
플라스크에 의해 흡수된 열량 : 115.6g * 0.85J/g˙℃ * 2.5℃ = 245.65J
반응 1에서 방출된 열량 : 용액에 의하여 흡수된 열량 + 플라스크에 의해 흡수된 열량
∴ 2084.78J + 245.65J = 2330.43J
NaOH 1몰의 반응열 : 0.05 mol/L : 2330.43 J = 1 mol/L : x J
∴ x = 46608.6 J/mol
삼각플라스크의 무게
115.6g
온도변화 (∆T)
2.5∘c
고체 NaOH 의 무게
2.00g
용액에 의해 흡수된열량
199.5*4.18*2.5 =2084.78J
NaOH의 몰농도
0.05 mol/L
플라스크에 의해 흡수된열량
115.6*0.85*2.5 =245.65J
최종(중화된 후)무게
199.5g
초기온도(HCl만 존재)
21.5℃
반응에서 방출된열량
2330.43J
나중온도(중화된 후)
24℃
NaOH 1몰의 반응열
46608.6 J/mol
• 반응(3)의 실험 결과 값
용액에 의하여 흡수된 열량 : 188.08g * 4.18J/g˙℃ * 2℃ = 1572.35 J
플라스크에 의해 흡수된 열량 : 109.8g * 0.85J/g˙℃ * 2℃ = 186.66 J
반응 3에서 방출된 열량 : 용액에 의하여 흡수된 열량 + 플라스크에 의해 흡수된 열량
- 참고문헌
-
①단위조작실험 학연사 고완석 저
②단위조작실험 형설출판사 김병규 저
자료평가
-
아직 평가한 내용이 없습니다.










