[일반화학 실험] 일반화학 실험 - 화학반응속도 예비, 결과 보고서
 등록일 / 수정일
등록일 / 수정일 페이지 / 형식
페이지 / 형식 자료평가
자료평가 구매가격
구매가격
- 2008.09.05 / 2019.12.24
- 6페이지 /
 hwp (아래아한글97)
hwp (아래아한글97) 



 1건 (구매금액의 3%지급)
1건 (구매금액의 3%지급)-
1,000원
 800원
800원
최대 20페이지까지 미리보기 서비스를 제공합니다.
자료평가하면 구매금액의 3%지급!
 1
1 2
2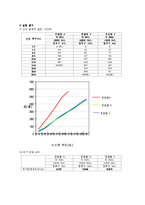 3
3 4
4 5
5 6
6
추천 연관자료
- 하고 싶은 말
- 일반화학 및 실험1에서 실험한는 화학반응속도 측정 실험(과산화수소 분해 반응: 촉매 KI-요오드화칼륨)에 대한 예비 결과 보고서입니다
- 목차
-
1. 실험 목적
2. 실험 이론
3. 실험 기구 및 시약
4. 실험 방법
5. 주의 및 참고사항
6. 실험 결과
7. 토의
- 본문내용
-
1. 실험 목적
화학 반응의 속도식을 나타내는 데에 필요한 속도 상수와 반응 차수를 실험적으로 결정한다.
2. 실험 이론
일반적으로 반응속도는 반응 물질의 농도에 의존하기 때문에 다음과 같은 속도식으로 표현한다.
aA + bB -> cC + dD
k= Rate constant (온도에 의존)
m ,n = Reaction order (실험을 통해서만 결정)
이 실험에서는 과산화수소(H2O2)가 물과 산소 기체로 분해되는 반응 속도를 측정한다.
이 분해 반응의 속도는 상온에서 매우 느리지만 KI를 촉매로 넣어주면 반응 속도가 상당히 빨라진다.
반응:
따라서 첫 번째 단계가 속도결정단계가 되며 전체 반응 속도는 다음과 같다.
과산화수소의 분해 반응은 인 자발적인 반응이고 대기압에서는 Ea = 76kj/mol 인 상당히 느린 반응이다. 반응물이 생성물로 가기 위해서 분자들은 활성화 에너지를 넘을 수 있는 충분한 열에너지를 가져야 한다. 주어진 온도에서 분자들은 확정 에너지 분포를 보이는데 모든 분자들의 평균 열에너지는 RT에 비례한다. 분자들 중에서 Ea 이상의 에너지를 가지는 분자들의 분율은 활성화에너지와 열에너지의 비(Ea/RT)에 지수적으로 의존하고 이러한 수학적 관례는 다음 식으로 표현한다.
요오드 이온은 반응물과 같은 상을 갖는 균일 촉매로 활성화 에너지를 76kj/mol에서 57kj/mol 로 낮추어 줌으로써 물과 산소의 생성을 촉진한다,
실험은 시간에 따른 산소 기체의 발생량을 그래프로 나타내어서 그 기울기로부터 반응 속도를 알아낸다.
- 참고문헌
- 표준 일반 화학 실험. 대한 화학회. 천문각
자료평가





- 계산과정, 수식 체계적으로 정리되어 있어서 좋아요
- ekh***
(2013.09.14 18:26:34)
오늘 본 자료
더보기

최근 판매 자료
- [분석화학실험] EDTA Titration (우유속의 칼슘정량) 결과레포트
- [정보통신,통신이론,솔루션,연습문제] 통신 이론 2장 솔루션 전부다
- 이재수 수문학(구미서관) 연습문제 2장
- 충북대_일반물리학및실험1_7주차_역학적에너지보존
- 전공면접, 전공 PT 면접 대비 - 기계공학과 전공 면접 기출 질문 모음(건설, 엔지니어링 등)
- [공학]토질공식
- 화학실험보고서 - 이산화탄소의 분자량
- 정보통신학개론_현재 스마트폰은 컴퓨터와 전화기의 기능이 융복합화된 IT기술의 총화라고 할 수 있습니다 본인이 가지고 있는 (관심있는) 스마트폰을 먼저 선정한 후 그 스마트폰의 사양과 특징 그리고 사용된 기술들에 대해 공부하고 조사정리한 내용을 제출하면 됩니다
- [일반화학실험보고서] 일반화학실험보고서-이산화탄소분자량
- 철근 인장강도 실험 결과 및 분석
저작권 관련 사항 정보 및 게시물 내용의 진실성에 대하여 레포트샵은 보증하지 아니하며, 해당 정보 및 게시물의 저작권과 기타 법적 책임은 자료 등록자에게 있습니다. 위 정보 및 게시물 내용의 불법적 이용, 무단 전재·배포는 금지됩니다. 저작권침해, 명예훼손 등 분쟁요소 발견시 고객센터에 신고해 주시기 바랍니다.









