[화학] 7장 화합물의 정량적 조성
 등록일 / 수정일
등록일 / 수정일 페이지 / 형식
페이지 / 형식 자료평가
자료평가 구매가격
구매가격
- 2008.05.22 / 2019.12.24
- 13페이지 /
 ppt (파워포인트 2003)
ppt (파워포인트 2003) - 평가한 분이 없습니다. (구매금액의 3%지급)
- 1,100원
최대 20페이지까지 미리보기 서비스를 제공합니다.
자료평가하면 구매금액의 3%지급!
 1
1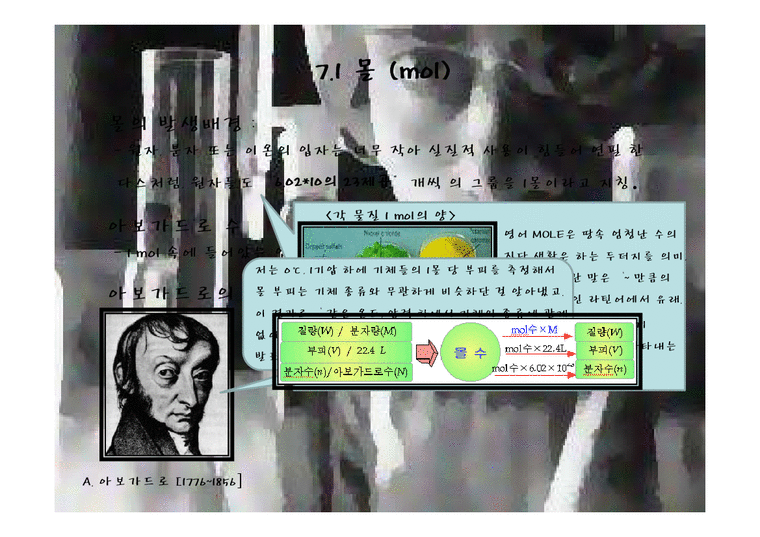 2
2 3
3 4
4 5
5 6
6 7
7 8
8 9
9 10
10 11
11 12
12 13
13
추천 연관자료
- 목차
-
7.1 몰 (mol)
7.2 화합물의 몰 질량
7.3 화합물의 조성백분율이란?
7.4 실험식 & 분자식
7.5 실험식 계산
7.6 실험식에서 분자식 계산
- 본문내용
-
7.1 몰 (mol)
몰의 발생배경 :
- 원자, 분자 또는 이온의 입자는 너무 작아 실질적 사용이 힘들어 연필 한 다스처럼, 원자들도 “ ”개씩 의 그룹을 1몰이라고 지칭.
아보가드로 수
- 1 mol 속에 들어있는 입자의 수, N 으로 표시. (6.022×1023 개)
아보가드로의 법칙
<각 물질 1 mol의 양>
영어 MOLE은 땅속 엄청난 수의
집단 생활은 하는 두더지를 의미,
몰(MOLE)이란 말은‘~ 만큼의
묶음’의 뜻인 라틴어에서 유래.
현재 국제 표준 단위 체계
(SI)에서 물질의 양을 나타내는
단위로 사용.
저는 0℃, 1기압 하에 기체들의 1몰 당 부피를 측정해서
몰 부피는 기체 종류와 무관하게 비슷하단 걸 알아냈고.
이 결과로‘ 같은 온도, 압력 하에서 기체의 종류에 관계
없이 같은 부피 속엔 같은 수의 분자가 들어있다.’ 라고
발표했지요
자료평가
-
아직 평가한 내용이 없습니다.










